题目内容
已知:H2(g)+![]() O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH2=-2 220.0 kJ·mol-1
实验测得H2和C3H8共5 mol,完全燃烧生成液态水时放热5 297.4 kJ.则混合气体中H2和C3H8的体积比是________.已知H2O(l)=H2O(g) ΔH=44 kJ·mol-1,则丙烷燃烧生成CO2和水蒸气的热化学方程式为________________.
答案:
解析:
解析:
|
3∶2 C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2 044.0 kJ·mol-1 |

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.请回答下列问题:
(1)2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2599kJ?mol-1,则乙炔的燃烧热为 .
(2)有些反应进行得很慢,有些反应不容易直接发生,有些反应的产品不纯(有副反应发生),这给测定反应热造成了困难,此时可利用盖斯定律,就可以间接地把它们的反应热计算出来.已知
①CO(g)+
O2(g)═CO2(g)△H1=-283.0kJ?mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
则C(s)+
O2(g)=CO(g)△H= .
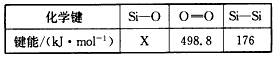
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.已知键能数据如表.
反应N2+3H2?2NH3△H=a kJ?mol-1.试根据表中所列键能数据估算a= .
(1)2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2599kJ?mol-1,则乙炔的燃烧热为
(2)有些反应进行得很慢,有些反应不容易直接发生,有些反应的产品不纯(有副反应发生),这给测定反应热造成了困难,此时可利用盖斯定律,就可以间接地把它们的反应热计算出来.已知
①CO(g)+
| 1 |
| 2 |
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
则C(s)+
| 1 |
| 2 |
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.已知键能数据如表.
| 化学键 | 键能(kJ/mol) | 化学键 | 键能(kJ/mol) |
| N≡N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 |
 已知:H2(g)+
已知:H2(g)+ 已知:H2(g)+
已知:H2(g)+