题目内容
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海藻中提取碘的过程如下:
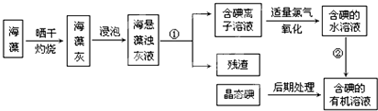
请填写下列空白:
(1)灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是 . (从下列仪器中选出所需的仪器,用标号字母填写在空白处).
A.烧杯 B.瓷坩埚 C.表面皿 D.泥三角 E.酒精灯 F.坩埚钳
(2)指出提取碘的过程中有关的实验操作名称:① 、② .
(3)提取碘的过程中,不能使用的有机溶剂是 .其原因是 .
A.酒精 B.苯 C.汽油
该提取操作通常在 (仪器名称)中进行,若得到的是含碘的四氯化碳溶液,静置后分层,下层为 色.
(4)设计一个简单的实验,检验提取碘后的水溶液中是否还含有单质碘.请写出该实验的实验步骤、现象及结论 .
(5)加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.
(Ⅰ)测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全.则加碘食盐样品中的碘元素含量是 mg/kg.(以含w的代数式表示).
(已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-.)
(Ⅱ)学生乙又进行了下列实验:
①请推测实验中产生蓝色现象的可能原因,用离子方程式表示 .
②根据学生乙的实验结果,请对学生甲的实验结果作出简要评价: .

请填写下列空白:
(1)灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.瓷坩埚 C.表面皿 D.泥三角 E.酒精灯 F.坩埚钳
(2)指出提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程中,不能使用的有机溶剂是
A.酒精 B.苯 C.汽油
该提取操作通常在
(4)设计一个简单的实验,检验提取碘后的水溶液中是否还含有单质碘.请写出该实验的实验步骤、现象及结论
(5)加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.
(Ⅰ)测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全.则加碘食盐样品中的碘元素含量是
(已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-.)
(Ⅱ)学生乙又进行了下列实验:
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡. | 溶液变蓝色 |
②根据学生乙的实验结果,请对学生甲的实验结果作出简要评价:
考点:海带成分中碘的检验,探究物质的组成或测量物质的含量
专题:
分析:I、(1)根据实验操作步骤①灼烧来分析用到的实验仪器;
(2)①分离固体和液体用过滤,②利用溶解性的差异判断操作方法;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;萃取所用的主要仪器是分液漏斗;利用四氯化碳的密度大于水来分析;(4)利用碘单质遇淀粉变蓝来检验碘的存在;
(5)根据Na2S2O3与KIO3反应的关系式来计算KIO3的物质的量,再根据质量分数公式来计算碘的含量;
II、①酸性条件下,碘离子被氧气氧化生成碘单质;
②过量的碘离子易被空气氧化生成碘单质.
(2)①分离固体和液体用过滤,②利用溶解性的差异判断操作方法;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;萃取所用的主要仪器是分液漏斗;利用四氯化碳的密度大于水来分析;(4)利用碘单质遇淀粉变蓝来检验碘的存在;
(5)根据Na2S2O3与KIO3反应的关系式来计算KIO3的物质的量,再根据质量分数公式来计算碘的含量;
II、①酸性条件下,碘离子被氧气氧化生成碘单质;
②过量的碘离子易被空气氧化生成碘单质.
解答:
解:(1)灼烧固体物质一般使用(瓷)坩埚,而坩埚的取放用坩埚钳,坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯.故答案为:BDEF;
(2)①分离固体和液体用过滤,②将碘单质从水溶液中提取出来,应利用碘单质在有机溶剂中的溶解度比在水中的溶解度大的特点来实现,即用有机溶剂将碘单质从水溶液中萃取出来,
故答案为:过滤;萃取;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,从题给信息可知,酒精和水互溶,不能用作萃取剂,苯和与汽油水互不相溶,故可用苯或汽油做萃取剂;萃取所用的主要仪器是分液漏斗;四氯化碳的密度大于水,故萃取后下层是碘的四氯化碳溶液,呈紫红色.
故答案为:A,酒精与水互溶,分液漏斗,紫(红)色;
(4)碘单质遇淀粉变蓝,故要想检验提取碘后的水溶液中是否还含有单质碘,只需向溶液中加入淀粉溶液,观察是否变蓝即可,故答案为:取少量提取液于试管中,滴加淀粉溶液,若溶液显蓝色,则说明原提取液中有碘单质;
(5)设碘酸钾的物质的量为x.KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O①;
I2+2S2O3 2-=2I-+S4 O62-②,将方程式②×3+①得
IO3-+6H++6S2O32-=I-+3S4O62-+3H2O
1 6
x 2.0×10-3mol/L×0.01L
x=
=
×10-5mol,根据碘原子守恒知,碘原子的质量=
×10-5mol×127g/mol=
×10-5g,所以碘元素的质量分数=
×100%=
mg/kg,
故答案为:
;
II、①酸性条件下,碘离子被氧气氧化生成碘单质,离子反应方程式为:4I-+4H++O2=2I2+2H2O,故答案为:4I-+4H++O2=2I2+2H2O;
②酸性条件下,过量的碘离子易被空气中氧气氧化生成碘单质,导致测定结果偏大,故答案为:学生甲实验结果会偏大.
(2)①分离固体和液体用过滤,②将碘单质从水溶液中提取出来,应利用碘单质在有机溶剂中的溶解度比在水中的溶解度大的特点来实现,即用有机溶剂将碘单质从水溶液中萃取出来,
故答案为:过滤;萃取;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,从题给信息可知,酒精和水互溶,不能用作萃取剂,苯和与汽油水互不相溶,故可用苯或汽油做萃取剂;萃取所用的主要仪器是分液漏斗;四氯化碳的密度大于水,故萃取后下层是碘的四氯化碳溶液,呈紫红色.
故答案为:A,酒精与水互溶,分液漏斗,紫(红)色;
(4)碘单质遇淀粉变蓝,故要想检验提取碘后的水溶液中是否还含有单质碘,只需向溶液中加入淀粉溶液,观察是否变蓝即可,故答案为:取少量提取液于试管中,滴加淀粉溶液,若溶液显蓝色,则说明原提取液中有碘单质;
(5)设碘酸钾的物质的量为x.KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O①;
I2+2S2O3 2-=2I-+S4 O62-②,将方程式②×3+①得
IO3-+6H++6S2O32-=I-+3S4O62-+3H2O
1 6
x 2.0×10-3mol/L×0.01L
x=
| 2.0×10-5 |
| 6 |
| 1 |
| 3 |
| 1 |
| 3 |
| 127 |
| 3 |
| ||
| Wg |
| 1270 |
| 3W |
故答案为:
| 1270 |
| 3W |
II、①酸性条件下,碘离子被氧气氧化生成碘单质,离子反应方程式为:4I-+4H++O2=2I2+2H2O,故答案为:4I-+4H++O2=2I2+2H2O;
②酸性条件下,过量的碘离子易被空气中氧气氧化生成碘单质,导致测定结果偏大,故答案为:学生甲实验结果会偏大.
点评:本题考查了氧化还原反应方程式的配平及有关计算,计算时注意是求食盐中碘的含量不是碘酸钾的含量,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
NA 代表阿伏加德罗常数的数值,下列说法中错误的是( )
| A、2.4g金属镁变为镁离子时失去的电子数为0.2NA |
| B、1.8g 水所含电子数为NA |
| C、16g O2和O3的混合气,所含的氧原子数为NA |
| D、22.4L氢气含有的原子数为2NA |
下列各组微粒中,互为同位素的是( )
A、
| ||||
| B、H2O和H2O2 | ||||
| C、红磷和白磷 | ||||
| D、甲烷和乙烷 |
 下表是元素周期表一部分,表中所列字母分别代表某一化学元素.
下表是元素周期表一部分,表中所列字母分别代表某一化学元素.