题目内容
下列化学方程式或离子方程式正确的是( )
| A、常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O |
| B、向碳酸氢钠溶液中加入少量盐酸:CO32-+2H+═CO2↑+H2O |
| C、向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ |
| D、向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.常温下,铁和浓硝酸发生钝化现象;
B.碳酸氢钠在水溶液里电离出碳酸氢根离子;
C.二者反应还生成弱电解质一水合氨;
D.二者反应生成硝酸铜、二氧化氮和水.
B.碳酸氢钠在水溶液里电离出碳酸氢根离子;
C.二者反应还生成弱电解质一水合氨;
D.二者反应生成硝酸铜、二氧化氮和水.
解答:
解:A.常温下,铁和浓硝酸发生钝化现象,所以不写离子方程式,故A错误;
B.碳酸氢钠在水溶液里电离出碳酸氢根离子,离子方程式为HCO3-+H+═CO2↑+H2O,故B错误;
C.二者反应还生成弱电解质一水合氨,离子方程式为2OH-+2NH4++Ba2++SO42-=BaSO4↓+2NH3.H2O,故C错误;
D.二者反应生成硝酸铜、二氧化氮和水,离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故D正确;
故选D.
B.碳酸氢钠在水溶液里电离出碳酸氢根离子,离子方程式为HCO3-+H+═CO2↑+H2O,故B错误;
C.二者反应还生成弱电解质一水合氨,离子方程式为2OH-+2NH4++Ba2++SO42-=BaSO4↓+2NH3.H2O,故C错误;
D.二者反应生成硝酸铜、二氧化氮和水,离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故D正确;
故选D.
点评:本题考查离子方程式正误判断,明确离子性质及离子之间的反应是解本题关键,注意要遵循客观事实、原子守恒、电荷守恒及转移电子守恒,易错选项是C.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在4NH4+5O2?4NO+6H2O反应中,表示该反应速率最快的是( )
| A、υ(NH4)=0.8 mol/(L?s) |
| B、υ(O2)=1.0 mol/(L?s) |
| C、υ(NO)=1.0 mol/(L?s) |
| D、υ(H2O)=1.8 mol/(L?s) |
与22g二氧化碳所含氧原子数相等的水的质量是( )
| A、9g | B、22g |
| C、44 g | D、18g |
下列物质加入水中显著放热的是( )
| A、浓硫酸 |
| B、固体NaCl |
| C、无水乙醇 |
| D、固体NH4NO3 |
下列离子方程式的书写正确的是( )
| A、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| B、铁和稀硝酸反应:Fe+2H+=H2↑+Fe2+ |
| C、向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| D、实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |
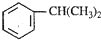 是一种重要的有机化工原料.根据题意完成下列
是一种重要的有机化工原料.根据题意完成下列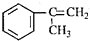 是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法
是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法