题目内容
铊是超导材料的组成元素之一,铊在元素周期表中位于第六周期,与铝是同主族元素,元素符号是Tl.以下对铊的单质及其化合物的性质推断中,不正确的是( )
| A、铊是易导电的银白色金属 |
| B、铊能生成+3价的离子 |
| C、Tl3+的氧化能力比Al3+强 |
| D、氢氧化铊的碱性比氢氧化铝强 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,利用同主族元素的性质变化规律来解答.
解答:
解:A.铝为银白色金属,Tl与Al同主族,则铊是易导电的银白色金属,故A正确;
B.第ⅢA族的最高价为+3,且为金属元素,则能生成+3价离子化合物,故B正确;
C.金属性Tl>Al,则Tl3+的氧化能力比Al3+弱,故C错误;
D.同主族从上到下金属性增强,则Tl(OH)3碱性比氢氧化铝强,故D正确.
故选C.
B.第ⅢA族的最高价为+3,且为金属元素,则能生成+3价离子化合物,故B正确;
C.金属性Tl>Al,则Tl3+的氧化能力比Al3+弱,故C错误;
D.同主族从上到下金属性增强,则Tl(OH)3碱性比氢氧化铝强,故D正确.
故选C.
点评:本题考查元素的性质,为高频考点,侧重于学生的分析能力的考查熟悉元素在周期表中的位置及元素周期律是解答本题的关键,难度不大.

练习册系列答案
相关题目
已知:HCN(aq)+NaOH(aq)═NaCN(aq)+H2O(l)△H=-12.1kJ?mol-1;
HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-55.6kJ?mol-1
则HCN在水溶液中电离的△H等于( )
HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-55.6kJ?mol-1
则HCN在水溶液中电离的△H等于( )
| A、+43.5 kJ?mol-1 |
| B、+67.7 kJ?mol-1 |
| C、-43.5 kJ?mol-1 |
| D、-67.7 kJ?mol-1 |
下列各组物质按酸、碱、盐分类顺序排列,正确的是( )
| A、硫酸,纯碱(Na2CO3),石灰石 |
| B、醋酸,烧碱(Na OH),硫酸铜 |
| C、硝酸,熟石灰,苛性钾(KOH) |
| D、醋酸,小苏打(NaHCO3),熟石灰(Ca(OH)2) |
化学平衡问题研究对象主要是( )
| A、化学反应 | B、可逆反应 |
| C、离子反应 | D、气态物质的反应 |
达平衡状态的可逆反应:N2(g)+3H2(g)?2NH3(g),改变某一条件,一段时间后,测得正反应速率以N2的浓度减小表示:v(N2)=0.6mol/(L?min),逆反应速率以NH3的浓度减小表示:v(NH3)=1.2mol/(L?min),此时可逆反应的状态是( )
| A、测定时,v正>v逆 |
| B、测定时,v正<v逆 |
| C、测定时,v正=v逆 |
| D、不可能达到新平衡 |
下列各组离子能在溶液中大量共存的是( )
| A、K+、Ag+、NO3-、S2- |
| B、Na+、Al3+、SO42-、HCO3- |
| C、NH4+、K+、OH-、SO42- |
| D、H+、Fe3+、Cl-、NO3- |
在水中存在H2O?H++OH-平衡,加入下列哪种物质或进行哪项操作,不会使平衡发生移动( )
| A、加入NaOH固体 |
| B、加入NaCl固体 |
| C、加入CH3COOH固体 |
| D、升温 |
将一定量的锌与100mL 18.5mol/L浓硫酸充分反应,锌完全溶解,同时生成16.8L气体(标准状况),将反应后的溶液稀释到1L,测得溶液的c(H+)=1mol/L,则下列叙述中错误的是( )
| A、气体A为二氧化硫和氢气的混合物 |
| B、气体A中二氧化硫和氢气的体积比为4:1 |
| C、反应中共消耗锌95.5g |
| D、反应中共转移电子1.5mol |
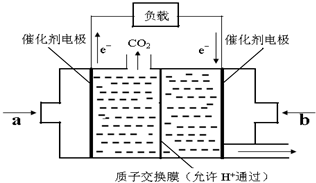 随着世界工业经济的发展、人口的剧增,全球能源紧张面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率.
随着世界工业经济的发展、人口的剧增,全球能源紧张面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率.