题目内容
下列因果关系叙述正确的是( )
| A、纯碱是一种碱,故可用于去油污 |
| B、SiO2能与氢氟酸及碱反应,故SiO2是两性氧化物 |
| C、Na的金属性比Mg强,故可用Na与MgCl2溶液反应制取Mg |
| D、浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
考点:钠的重要化合物,硝酸的化学性质,硅和二氧化硅,钠的化学性质
专题:元素及其化合物
分析:A.纯碱是碳酸钠,属于盐;
B.两性氧化物是指:能够与碱和酸反应反应,都生成盐和水的氧化物;
C.钠投入到盐溶液中,先与水发生反应;
D.浓硝酸不稳定,见光分解生成二氧化氮,二氧化氮溶于硝酸而使硝酸显黄色.
B.两性氧化物是指:能够与碱和酸反应反应,都生成盐和水的氧化物;
C.钠投入到盐溶液中,先与水发生反应;
D.浓硝酸不稳定,见光分解生成二氧化氮,二氧化氮溶于硝酸而使硝酸显黄色.
解答:
解:A.纯碱是一种盐,故A错误;
B.二氧化硅与氢氟酸反应生成物不是盐和水,不属于两性氧化物,故B错误;
C.钠投入到盐溶液中,先与水发生反应,不能从溶液中置换镁,故C错误;
D.浓硝酸不稳定,见光分解生成二氧化氮,二氧化氮溶于硝酸而使硝酸显黄色,故D正确;
故选:D.
B.二氧化硅与氢氟酸反应生成物不是盐和水,不属于两性氧化物,故B错误;
C.钠投入到盐溶液中,先与水发生反应,不能从溶液中置换镁,故C错误;
D.浓硝酸不稳定,见光分解生成二氧化氮,二氧化氮溶于硝酸而使硝酸显黄色,故D正确;
故选:D.
点评:本题考查了元素化合物知识,为高考热门考点,侧重基础知识的考查,明确物质的性质是解题关键,注意两性氧化物的概念,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
A、因为Na2CO3+SiO2
| ||||
| B、碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似 | ||||
| C、二氧化硅既溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物 | ||||
| D、二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不能和水反应生成硅酸 |
已知:
①硫酸比次氯酸稳定;
②高氯酸是比硫酸更强的酸;
③S2-易被氯气氧化;
④氯化氢比硫化氢稳定;
⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应;
⑥浓盐酸有挥发性,浓H2SO4无挥发性,
上述中能说明氯元素的非金属性比硫元素强的是( )
①硫酸比次氯酸稳定;
②高氯酸是比硫酸更强的酸;
③S2-易被氯气氧化;
④氯化氢比硫化氢稳定;
⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应;
⑥浓盐酸有挥发性,浓H2SO4无挥发性,
上述中能说明氯元素的非金属性比硫元素强的是( )
| A、①②③ | B、②③④ |
| C、③④⑤ | D、④⑤⑥ |
我国拥有较丰富的地热资源,其开发利用前景广阔.下列关于地热能说法正确的是( )
①可以用于洗浴、发电以及供暖等方面
②与煤炭、石油、天然气一样都是化石资源
③主要源于地球内部放射性元素衰变产生的能量
④与地下水结合可形成热水型,释放形式之一是温泉.
①可以用于洗浴、发电以及供暖等方面
②与煤炭、石油、天然气一样都是化石资源
③主要源于地球内部放射性元素衰变产生的能量
④与地下水结合可形成热水型,释放形式之一是温泉.
| A、①②③ | B、①②④ |
| C、①③④ | D、②③④ |
某反应体系中存在下列六种物质:As2S3、HNO3、H2SO4、NO、H3AsO4和H2O,已知其中As2S3是反应物之一.下列说法不正确的是( )
| A、该反应属于氧化还原反应 |
| B、此反应中只有砷元素被氧化,只有氮元素被还原 |
| C、HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物 |
| D、HNO3、H2SO4、H3AsO4都是最高价氧化物对应的水化物 |
下列叙述正确的是( )
| A、HClO可以使有色物质漂白,所以具有氧化性物质可作漂白剂 |
| B、Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C、浓硝酸中的HNO3,见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| D、因为SO2具有较强还原性,所以不能用浓硫酸来干燥它 |
下列物质的电子式书写正确的是( )
A、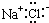 |
B、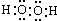 |
C、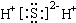 |
D、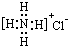 |