题目内容
工业生产中物质的循环利用有多种模式.例如:

表述不正确的是( )

表述不正确的是( )
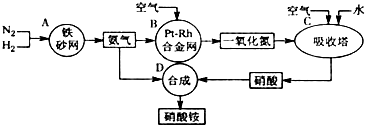
| A、若图I为合成氨,则其中N2、H2可循环使用 |
| B、若图I为合成SO3,则其中SO2、O2可循环使用 |
| C、若图Ⅱ为电解熔融MgCl2得到镁,则其中HCl可循环使用 |
| D、若图Ⅲ为氨氧化法制硝酸,则其中NO2可循环使用 |
考点:工业合成氨,工业制取硫酸,工业制取硝酸,电解原理
专题:元素及其化合物
分析:A、图Ⅰ若是工业合成氨,反应是化学平衡,不能进行彻底,原料气可以循环利用;
B、图Ⅰ中SO2和O2生成SO3,反应是化学平衡,不能进行彻底,原料气可以循环利用;
C、海水提取得到氢氧化镁和盐酸反应生成氯化镁,浓缩蒸发得到氯化镁固体,电解得到金属镁和氯气,氯气和氢气反应生成氯化氢可以循环利用;
D、图Ⅲ可表示氨催化氧化法制硝酸时,氨气和氧气催化氧化为一氧化氮,一氧化氮氧化为二氧化氮,二氧化氮溶于水生成硝酸和一氧化氮,一氧化氮可以循环利用.
B、图Ⅰ中SO2和O2生成SO3,反应是化学平衡,不能进行彻底,原料气可以循环利用;
C、海水提取得到氢氧化镁和盐酸反应生成氯化镁,浓缩蒸发得到氯化镁固体,电解得到金属镁和氯气,氯气和氢气反应生成氯化氢可以循环利用;
D、图Ⅲ可表示氨催化氧化法制硝酸时,氨气和氧气催化氧化为一氧化氮,一氧化氮氧化为二氧化氮,二氧化氮溶于水生成硝酸和一氧化氮,一氧化氮可以循环利用.
解答:
解:A、图Ⅰ若是工业合成氨,反应是化学平衡,不能进行彻底,原料气氮气和氢气可以循环利用,故A正确;
B、若图I为合成SO3,SO2和O2生成SO3,反应是化学平衡,不能进行彻底,原料气可以循环利用,故B正确;
C、海水提取得到氢氧化镁和盐酸反应生成氯化镁,浓缩蒸发得到氯化镁固体,电解得到金属镁和氯气,氯气和氢气反应生成氯化氢可以循环利用,故C正确;
D、图Ⅲ可表示氨催化氧化法制硝酸时,氨气和氧气催化氧化为一氧化氮,一氧化氮氧化为二氧化氮,二氧化氮溶于水生成硝酸和一氧化氮,一氧化氮可以循环利用,故D错误;
故选D.
B、若图I为合成SO3,SO2和O2生成SO3,反应是化学平衡,不能进行彻底,原料气可以循环利用,故B正确;
C、海水提取得到氢氧化镁和盐酸反应生成氯化镁,浓缩蒸发得到氯化镁固体,电解得到金属镁和氯气,氯气和氢气反应生成氯化氢可以循环利用,故C正确;
D、图Ⅲ可表示氨催化氧化法制硝酸时,氨气和氧气催化氧化为一氧化氮,一氧化氮氧化为二氧化氮,二氧化氮溶于水生成硝酸和一氧化氮,一氧化氮可以循环利用,故D错误;
故选D.
点评:本题考查了物质的循环利用有的多种模式,物质转化关系,工业制备的流程,反应原理的应用,主要是工业合成氨、海水提取镁、氨的催化氧化制硝酸的生产原理和反应特征的熟练掌握,题目较综合,难度较大,需要熟练掌握工业制备的流程.

练习册系列答案
相关题目
下列各组离子在给定条件下能大量共存的是( )
| A、常温下在pH=1的溶液中:NH4+、K+、HCO3-、Cl- |
| B、有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- |
| C、有NO-3存在的强酸性溶液中:NH+4、Ba2+、Fe2+、Br- |
| D、常温下在pH=13的溶液中:Na+、S2-、PO43-、SO32- |
下列物质按纯净物、混合物、电解质、非电解质的顺序组合正确的是( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 铜 |
| B | 胆矾 | 石灰水 | 硫酸钡 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠溶液 | 三氧化硫 |
| D | 冰醋酸 | 氢氧化铁胶体 | 苛性钾溶液 | 乙醇 |
| A、A | B、B | C、C | D、D |
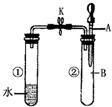 如图所示,试管①中盛有96℃的水,试管②中充满气体 B,将液体A滴入试管②中,充分反应后打开夹子K,发现试管①中的水立刻沸腾.则A与B可能是( )
如图所示,试管①中盛有96℃的水,试管②中充满气体 B,将液体A滴入试管②中,充分反应后打开夹子K,发现试管①中的水立刻沸腾.则A与B可能是( )| A、水与氮气 |
| B、稀硫酸与一氧化碳 |
| C、浓氢氧化钠溶液与二氧化碳 |
| D、饱和食盐水与氯气 |
丙烷的燃烧热为△H=-a kJ/mol,有以下反应:
①C3H8(g)=C3H6(g)+H2(g)△H=+b kJ/mol
②2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l)△H=-c kJ/mol
③2H2(g)+O2(g)=2H2O(l)△H=-d kJ/mol (b、c、d均为正值)则正确的( )
①C3H8(g)=C3H6(g)+H2(g)△H=+b kJ/mol
②2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l)△H=-c kJ/mol
③2H2(g)+O2(g)=2H2O(l)△H=-d kJ/mol (b、c、d均为正值)则正确的( )
| A、2a=c-d-2b |
| B、a=c-d-2b |
| C、2a=c+d-2b |
| D、a=c+d-b/2 |