题目内容
下列操作会引起实验误差的是( )
| A、进行中和滴定时,直接向刚洗净的锥形瓶中加待测液 |
| B、滴定未知浓度的盐酸所用的0.5mol?L-1 NaOH溶液时,用甲基橙为指示剂,在配制标准溶液时因与空气接触吸收了少量的CO2 |
| C、用标准NaOH溶液滴定未知浓度的稀H2SO4时,用酚酞作指示剂 |
| D、往用蒸馏水洗净的滴定管中直接加入待测液,再注入锥形瓶中 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.锥形瓶只能用蒸馏水洗涤,不能润洗;
B.如用甲基橙为指示剂,溶质只有NaCl,对实验没有影响;
C.酸碱的滴定,可用酚酞作指示剂;
D.滴定管应加待测液润洗,防止浓度偏低.
B.如用甲基橙为指示剂,溶质只有NaCl,对实验没有影响;
C.酸碱的滴定,可用酚酞作指示剂;
D.滴定管应加待测液润洗,防止浓度偏低.
解答:
解:A.锥形瓶只能用蒸馏水洗涤,不能润洗,否则导致误差偏大,故A不选;
B.甲基橙变色的PH范围是3.1~4.4,用甲基橙作指示剂滴定后溶液呈酸性,滴定时Na2CO3全部反应生成NaCl,对实验没有影响,故B不选;
C.酸碱的滴定,可用酚酞作指示剂,对实验没有影响,故C不选;
D.滴定管应加待测液润洗,防止浓度偏低,故D选.
故选D.
B.甲基橙变色的PH范围是3.1~4.4,用甲基橙作指示剂滴定后溶液呈酸性,滴定时Na2CO3全部反应生成NaCl,对实验没有影响,故B不选;
C.酸碱的滴定,可用酚酞作指示剂,对实验没有影响,故C不选;
D.滴定管应加待测液润洗,防止浓度偏低,故D选.
故选D.
点评:本题考查实验方案的评价,为高频考点,侧重学生的分析、实验能力的考查,主要把握酸碱中和滴定的实验原理和操作方法,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
若1mol 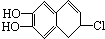 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )
 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )| A、1mol、2mol |
| B、2mol、3mol |
| C、3mol、2mol |
| D、3mol、3mol |
中草药秦皮中含有的七叶树内酯 (每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
 (每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A、2molBr2 2molNaOH |
| B、2molBr2 3molNaOH |
| C、3molBr2 4molNaOH |
| D、4molBr2 4molNaOH |
锌与100mL1mol/L盐酸反应的实验中,若设想向溶液中加入少量的①醋酸钠或②溴化铜或③醋酸铜(均为可溶性),并测定生成H2的速率(mL/min),预计三种方案的速率大小是( )
| A、①>③>② |
| B、③>②>① |
| C、②>③>① |
| D、①>②>③ |
下列气体中不能用排水法收集的是( )
| A、氢气 | B、氨气 | C、氧气 | D、氮气 |
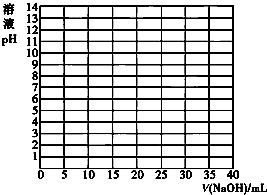 酸碱中和滴定常用于测定酸碱溶液的浓度.
酸碱中和滴定常用于测定酸碱溶液的浓度.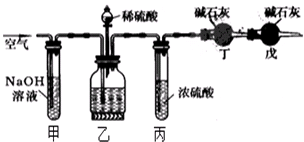 工业生产的纯碱中常含有少量的NaCl杂质,某校研究性活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.
工业生产的纯碱中常含有少量的NaCl杂质,某校研究性活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.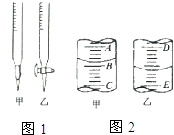 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空: