题目内容
13.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.回答下列问题:(1)基态砷原子的电子排布式为1s22s22p63s23p63d104s24p3.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间化学键类型为配位键,与CN-互为等电子体的化合物分子式为CO.
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染.光化学烟雾中含有NOx,、O3、CH2=CHCHO、HCOOH、
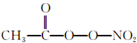 (PAN)等二次污染物.
(PAN)等二次污染物.①N2O结构式可表不为N=N=O,N2O中中心氮原子的杂化轨道类型为sp,l mol PAN中含σ键数目为10NA.
②测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr.Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个.晶胞中含K r原子为n个,则$\frac{m}{n}$=3(填数字).已知Kr晶体的密度为ρg/cm3,摩尔质量为Mg/mol.阿伏加德罗常数用NA表示,列式表示Kr晶胞参数α=$\root{3}{{\frac{4M}{{ρ{N_A}}}}}×{10^7}$nm.
分析 (1)Sn是33号元素,其原子核外有33个电子,根据构造原理书写其基态原子核外电子排布式;
(2)当中心原子有空轨道,配离子含有孤对电子时,能形成配位键;根据等电子体原理可写出与CN一互为等电子体的化合物分子式;
(3)根据氮原子的价层电子对数判断杂化方式,一个单键就是一个σ键,一个双键中含有一个σ键,一个π键;
(4)以顶点为计算,与之相邻的最近的Kr位于三个面心上,而顶点的原子为8个立方体共有,每个面心上的Kr为两个立方体共有,故与每个Kr原子相紧邻的Kr原子有3×4=12,晶胞中含Kr原子为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,然后求出比值;根据V=$\frac{m}{ρ}$求得晶胞的体积,进而可求得晶胞边长.
解答 解:(1)As的原子序数为33,电子分四层排布,最外层有5个电子,由构造原理可知电子排布为1s22s22p63s23p63d104s24p3(或[Ar]3d104s24p3);
故答案为:1s22s22p63s23p63d104s24p3(或[Ar]3d104s24p3);
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键类型为配位键,Fe3+有空轨道,能接受孤对电子,CN-能提供孤对电子,所以能形成配位键,与CN一互为等电子体的化合物分子式为 CO,
故答案为:配位; CO;
(3)在N=N=O中,边上的氮原子的价层电子对数为$\frac{5+1}{2}$=3,所以是sp2杂化,中间氮原子的价层电子对数为$\frac{5-1}{2}$=2,所以是sp杂化,根据 的结构可知,每个分子中含有10个σ键,所以1mol PAN中含σ键数目为10NA,
的结构可知,每个分子中含有10个σ键,所以1mol PAN中含σ键数目为10NA,
故答案为:sp2、sp;10NA;
(4)以顶点为计算,与之相邻的最近的Kr位于三个面心上,而顶点的原子为8个立方体共有,每个面心上的Kr为两个立方体共有,故与每个Kr原子相紧邻的Kr原子有3×4=12,晶胞中含Kr原子为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,所以m:n=12:4=3;根据V=$\frac{m}{ρ}$可知晶胞的体积为$\frac{\frac{4M}{{N}_{A}}}{ρ}$cm3=$\frac{4M}{ρ{N}_{A}}$cm3,所以晶胞边长a=$\root{3}{\frac{4M}{ρ{N}_{A}}}$cm=$\root{3}{\frac{4M}{ρ{N}_{A}}}$×107nm,
故答案为:3;$\root{3}{\frac{4M}{ρ{N}_{A}}}$×107.
点评 本题考查物质的结构与性质,注重对电子排布式、配位键、等电子体、原子杂化方式、晶胞的计算等知识,难度中等,注重基础知识的考查,侧重于考查学生的分析能力和对基础知识的综合应用考查.

 名校课堂系列答案
名校课堂系列答案| A. |  火法炼铜 | B. |  中和滴定 | C. |  酿酒 | D. |  制眼镜 |
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 硫酸工业生产中用水吸收SO3 | SO3可与水反应 | Ⅰ对,Ⅱ对,有 |
| B | 铝材可用作装修材料 | 金属铝的导电性好 | Ⅰ对,Ⅱ对,无 |
| C | 向锅炉中加入Na2CO3溶液有利于除去锅炉中的硫酸钙 | 硫酸钙比碳酸钙更难溶 | Ⅰ错,Ⅱ错,无 |
| D | 氮化硅可用于制造高温陶瓷 | 氮化硅的硬度大且熔点高 | Ⅰ对,Ⅱ对,有 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 硫酸工业的尾气中含有少量SO2,可用石灰水吸收,然后再用硫酸处理 | |
| B. | 工业上,常采用铁触媒催化剂,在400~500℃和10~30 MPa的条件下合成氨 | |
| C. | 造气中产生的CO,可在催化剂作用下,与水蒸气反应生成CO2和H2. | |
| D. | 在硫酸生产中,SO2催化氧化选择1~10 MPa、400~500℃条件下进行 |
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离常数 (25℃) | Ki=1.77×10-4 | Kii=2.98×10-6 | K1Ki1=4.3×10-7 Ki2=5.6×10-11 | Ki1=1.54×10-2 Ki2=5.6×10-7 |
(2)1molCl2与2molNa2CO3(aq)反应除生成NaCl外还有NaHCO3、NaClO(填化学式).
(3)向一定量的NaHCO3(aq)中通入少量的SO2(g),反应的离子方程式为HCO3-+SO2→HSO3-+CO2↑.
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性.
(4)将亚硒酸与高锰酸钾共热可制得硒酸(H2SeO4),配平该反应方程式,并标出电子转移
的方向和数目.
5H2SeO3+2KMnO4→1K2SeO4+2MnSeO4+2H2SeO4+3H2O
(5)与硫同族的元素Te,最高价氧化物的水化物碲酸(H6TeO6)的酸性比H2SO4弱(选填“强”或“弱”),其氧化性比硫酸强.向碲酸中通入SO2气体,若反应中生成的TeO2与Te的物质的量之比为2:1,写出该反应的化学方程式5SO2+3H6TeO6→2TeO2+Te+5H2SO4+4H2O.当6mol碲酸与一定量SO2恰好完全反应,所得溶液体积为20L,则所得溶液的pH为0.
| A. | 第一电离能:B>Be>Li | |
| B. | 电负性:F>N>O | |
| C. | Fe2+的最外层电子排布式为:3s23p63d6 | |
| D. | 基态铜原子的价电子排布图: |