题目内容
(12分)低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 850 |
平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)该反应逆反应的化学平衡常数表达式为K = 。
(2)上述正反应方向是 反应(填“放热”或“吸热”)。
(3)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如下图,则0~4 min的平均反应速率v(CO)= mol·L-1·min-1。

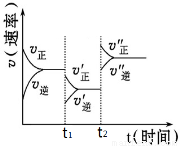
(4)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表。
①表中3 min~4 min之间反应处于 状态;C1数值 0.08 mol·L-1(填大于、小于或等于)。
②反应在4 min~5 min,平衡向逆方向移动,可能的原因是 (单选),表中5 min~6 min之间数值发生变化,可能的原因是 (单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
(5)若在500℃时进行,若CO、H2O的起始浓度均为0.020 mol·L-1,在该条件下,CO的最大转化率为: 。
(1)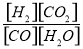 ;(2)放热;(3)0.03;(4)①平衡;大于;②D、A;(5)75%
;(2)放热;(3)0.03;(4)①平衡;大于;②D、A;(5)75%
【解析】
试题分析:(1)根据平衡常数的定义,该反应逆反应的化学平衡常数表达式为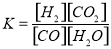 ;(2)升高温度,该反应平衡常数减小,所以正反应放热;(3)0~4 min的平均反应速率v(CO)
;(2)升高温度,该反应平衡常数减小,所以正反应放热;(3)0~4 min的平均反应速率v(CO)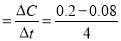 =0.03 mol·L-1·min-1;(4)①3 min~4 min时各物质的浓度均没变,所以处于平衡状态;850℃时,CO的平衡浓度为0.08 mol·L-1,升高温度,平衡左移,所以CO的平衡浓度增大,故C1数值大于0.08 mol·L-1;②4 min~5 min,CO、H2O的浓度都增大了0.036 mol·L-1,CO2的浓度减小0.036 mol·L-1,故改变的条件为增加氢气浓度;5 min~6 min CO浓度减小,H2O浓度增大,所以改变的条件为增加水蒸气;(5)500℃时K=9,设消耗的CO的浓度为x,则CO平衡浓度为(0.020—x) mol·L-1,H2O的平衡浓度为(0.020—x) mol·L-1,CO2的平衡浓度x、H2的平衡浓度x;
=0.03 mol·L-1·min-1;(4)①3 min~4 min时各物质的浓度均没变,所以处于平衡状态;850℃时,CO的平衡浓度为0.08 mol·L-1,升高温度,平衡左移,所以CO的平衡浓度增大,故C1数值大于0.08 mol·L-1;②4 min~5 min,CO、H2O的浓度都增大了0.036 mol·L-1,CO2的浓度减小0.036 mol·L-1,故改变的条件为增加氢气浓度;5 min~6 min CO浓度减小,H2O浓度增大,所以改变的条件为增加水蒸气;(5)500℃时K=9,设消耗的CO的浓度为x,则CO平衡浓度为(0.020—x) mol·L-1,H2O的平衡浓度为(0.020—x) mol·L-1,CO2的平衡浓度x、H2的平衡浓度x; ,x=0.015 mol·L-1,所以CO的最大转化率为
,x=0.015 mol·L-1,所以CO的最大转化率为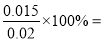 75%。
75%。
考点:本题考查化学反应速率、平衡常数、平衡转化率。

 阅读快车系列答案
阅读快车系列答案
 2NH3的能量变化如图所示,该反应的热化学方程式是
2NH3的能量变化如图所示,该反应的热化学方程式是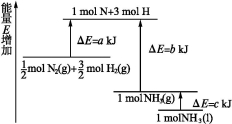
 2C(g)+3D(g),(正反应△H>0)的化学反应速率与化学平衡随外界条件改变而变化的关系图,下列条件的改变与图中情况相符的是:
2C(g)+3D(g),(正反应△H>0)的化学反应速率与化学平衡随外界条件改变而变化的关系图,下列条件的改变与图中情况相符的是: