题目内容
下列说法或表示方法中正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ/mol |
| C、测定中和热的实验中,NaOH要稍过量,以使HCl完全中和 |
| D、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)△H<0 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、硫蒸气变化为硫固体为放热过程;
B、氢气燃烧热的热化学方程式中氢气的化学计量数应为1;
C、氢氧化钠溶液稍过量,可以保证盐酸提供的氢离子完全反应;
D、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)该反应为吸热反应.
B、氢气燃烧热的热化学方程式中氢气的化学计量数应为1;
C、氢氧化钠溶液稍过量,可以保证盐酸提供的氢离子完全反应;
D、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)该反应为吸热反应.
解答:
解:A、硫蒸气变化为硫固体为放热过程,则等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量硫蒸气多,故A错误;
B、氢气的燃烧热热化学方程式为:H2(g)+
O2(g)=H2O(l)△H=-285.8 kJ/mol,故B错误;
C、测定中和热的实验中,NaOH要稍过量,保证盐酸提供的氢离子完全反应,故C正确;
D、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)该反应为吸热反应,△H>0,故D错误;
故选C.
B、氢气的燃烧热热化学方程式为:H2(g)+
| 1 |
| 2 |
C、测定中和热的实验中,NaOH要稍过量,保证盐酸提供的氢离子完全反应,故C正确;
D、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)该反应为吸热反应,△H>0,故D错误;
故选C.
点评:本题考查了反应热和焓变、燃烧热的热化学方程式的书写、中和热的测定以及常见的吸热反应和放热反应等,题目综合性较强,难度一般,注意反应热的分类和特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设 NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、16g CH4中含有10NA个电子 |
| B、1mol?L-1NaCl溶液含有NA个Na+ |
| C、1mol Cu和足量稀硝酸反应产生NA个NO分子 |
| D、常温常压下,22.4L CO2中含有NA个CO2分子 |
各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是( )
| A、用汽油除去衣服上的油污 |
| B、用餐具洗洁精清洗餐具上的油污 |
| C、用水洗去盘子中的水果渣 |
| D、用醋洗去水壶的水垢 |
下列说法中正确的一组是( )
| A、H2和D2互为同位素 |
B、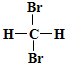 和 和 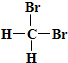 互为同分异构体 互为同分异构体 |
C、碳链为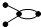 与 与 的烃为同系物 的烃为同系物 |
| D、金刚石、石墨互为同素异形体 |
根据下列某食品包装袋上的说明,下列关于此方便面的叙述中错误的是( )
| 品名 | ﹡﹡﹡牌红烧牛肉方便面 |
| 配料 | 小麦粉、牛肉、食盐、白砂糖、味精、棕榈油、脱水胡萝卜等 |
| 保质期 | 6个月 |
| 生产日期 | 2011年12月1日 |
| A、富含蛋白质的物质是牛肉 |
| B、富含油脂的物质是棕榈油 |
| C、此方便面现在已不能安全食用 |
| D、小麦粉中富含麦芽糖 |
t℃时,NaCl的溶解度为a g,取该温度下的饱和氯化钠溶液V mL,测得其密度为ρg/cm3,则下列表达式正确的是( )
A、w(NaCl)=
| ||
B、n(NaCl)=
| ||
C、c(NaCl)=
| ||
D、n(NaCl)=
|
某混合溶液中可能含有下列离子中的若干种:NH4+、Na+、Al3+、Fe2+、Fe3+、AlO2-、SO42-、I-、NO3-、CO32-,已知各离子的浓度均约为0.1mol/L,现取两份20mL该溶液进行如下实验:
①第一份加入足量盐酸,产生气体在空气中变为红色,在反应后的溶液中加入BaCl2溶液,有白色沉淀产生.
②第二份逐滴滴加NaOH溶液至过量,产生沉淀但不溶解,并有气体逸出.根据上述实验情况,以下说法错误的是( )
①第一份加入足量盐酸,产生气体在空气中变为红色,在反应后的溶液中加入BaCl2溶液,有白色沉淀产生.
②第二份逐滴滴加NaOH溶液至过量,产生沉淀但不溶解,并有气体逸出.根据上述实验情况,以下说法错误的是( )
| A、该混合溶液中一定不含有Fe3+、AlO2-、Al3+、CO32- |
| B、该混合溶液通过继续进行焰色反应可以间接确定是否含有I- |
| C、该混合溶液中肯定含有Fe2+、NH4+、SO42-、NO3- |
| D、向该混合溶液中滴加酚酞试液后呈红色 |
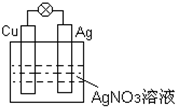 如右图所示
如右图所示