题目内容
14.下列说法正确的是( )| A. | NaCl、NH3、蔗糖分别属于强电解质、弱电解质、非电解质 | |
| B. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 | |
| C. | H2SO3(aq)+2NaOH(aq)=Na2SO3(aq)+2H2O(l)△H>-114.6 kJ/mol | |
| D. | 由石墨比金刚石稳定可推知:C(石墨)═C(金刚石)△H<0 |
分析 A、氨气在熔融状态下和水溶液中均不能导电;
B、化石燃料包括煤、石油和天然气;
C、在稀溶液中,强酸和强碱反应生成1mol水时放出的热量为中和热,△H=-57.3KJ/mol;
D、物质越稳定,能量越低.
解答 解:A、氨气在熔融状态下和水溶液中均不能导电,故氨气为非电解质,故A错误;
B、化石燃料包括煤、石油和天然气,植物油属于可再生燃料,故不是化石燃料,故B错误;
C、在稀溶液中,强酸和强碱反应生成1mol水时放出的热量为中和热,△H=-57.3KJ/mol,而亚硫酸为弱电解质,电离吸热,故H2SO3(aq)和2molNaOH(aq)反应生成2mol水时,放出的热量小于114.6KJ,则△H>-114.6 kJ/mol,故C正确;
D、物质越稳定,能量越低,故石墨的能量更低,则转化为金刚石要吸热,即△H>0,故D错误.
故选C.
点评 本题考查了电解质、非电解质和常见的化石燃料,应注意反应热△H的大小比较要带正负号比较,中和性较强,但难度不大.

练习册系列答案
相关题目
2.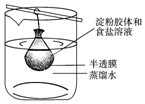 将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )
将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )
 将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )
将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )| A. | 烧杯内液体加入硝酸银溶液后有白色沉淀产生 | |
| B. | 烧杯内液体加入碘水后呈蓝色 | |
| C. | 袋内液体加入硝酸银溶液后不会出现白色沉淀 | |
| D. | 袋内液体加入碘水后不变蓝 |
9.配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是( )
| A. | 容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 | |
| B. | 配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸 | |
| C. | 配制1 L 0.1 mol•L-1的NaCl溶液时用托盘天平称量5.85 g NaCl固体 | |
| D. | 定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁 |
19.某有机物燃烧时,生成等物质的量的CO2和H2O,该有机物还能与新制Cu(OH)2悬浊液反应.则该有机物可能是( )
| A. | CH3CHO | B. | CH2═CHCOOH | C. | CH3CH2OH | D. | CH2═CHCHO |
3.在三个等体积的密闭容器中分别充入N2、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p),从大到小的顺序是( )
| A. | p(N2)>p(H2)>p(O2) | B. | p(O2)>p(N2)>p(H2) | C. | p(N2)>p(O2)>p(H2) | D. | p(H2)>p(N2)>p(O2) |
1.下列实验现象及相关的离子方程式均正确的是( )
| A. | 向FeCl3溶液中加入少量锌粒:2Fe3++Zn═2Fe2++Zn2+ | |
| B. | 向Ba(NO3)2溶液中通入SO2气体,出现白色沉淀:Ba2++SO2+H2O═BaSO3↓+2H+ | |
| C. | 向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2MnO4-+7H2O2+6H+═2Mn2++6O2↑+10H2O | |
| D. | 向FeCl3溶液中加入少量Na2S溶液:2Fe3++3S2-═Fe2S3↓ |
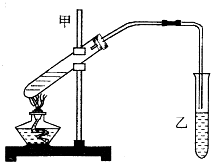 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: CH3COOC2H5+H2O.
CH3COOC2H5+H2O.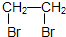 .
.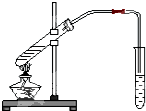 如图为实验室制乙酸乙酯的装置.
如图为实验室制乙酸乙酯的装置.