题目内容
13.下列各组混合物中,能用分液漏斗进行分离的是( )| A. | 酒精和水 | B. | 碘和四氯化碳 | C. | 水和四氯化碳 | D. | 汽油和乙醇 |
分析 能用分液漏斗进行分离的物质应互不相溶,结合常见物质的水溶性解答该题.
解答 解:酒精和水、汽油和乙醇、碘和四氯化碳都混溶,溶液不分层,而水和四氯化碳分层,可用分液的方法分离,
故选C.
点评 本题考查有机物的水溶性,为高频考点,侧重于学生的分析能力和实验能力的考查,题目难度不大,注意常见有机物的性质,特别是水溶性的特点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.实验室制备乙酸丁酯的叙述正确的是( )
| A. | 采用水浴加热法控制温度 | |
| B. | 采用边反应边蒸馏的方法提高产率 | |
| C. | 制取装置中有冷凝回流措施 | |
| D. | 用水和氢氧化钠溶液洗涤后分液分离出产品 |
4.镍氢电池已经成为混合动力汽车的主要电池类型.该电池放电时的总反应为:NiOOH+MH═Ni(OH)2+M,其中M表示储氢合金,MH表示吸附了氢原子的储氢合金,下列说法正确的是( )
| A. | 放电时负极反应为:MH+OH--e-═M+H2O | |
| B. | 放电时,每转移1mol电子,有1mol NiOOH被氧化 | |
| C. | 充电时正极反应为:NiOOH+H2O+e-═Ni(OH)2+OH- | |
| D. | 电池电解液可用KOH溶液,充电过程中KOH浓度减小 |
1.常温下,0.1mol/L的下列溶液酸性最强的是( )
| A. | NaHSO4 | B. | NaHSO3 | C. | Al2(SO4)3 | D. | CH3COOH |
8.下列各图所示的分子结构模型中,分子式为C6H6的是( )
| A. |  | B. |  | C. | 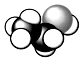 | D. | 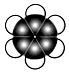 |
18.大规模开发利用铁、铜、铝,由早到晚的时间顺序是( )
| A. | 铜、铁、铝 | B. | 铁、铝、铜 | C. | 铝、铜、铁 | D. | 铁、铜、铝 |
5.用滴有酚酞和氯化钠溶液湿润的滤纸分别做甲、乙两个实验,下列判断错误的是( )

| A. | b极附近有气泡冒出 | B. | d极附近出现红色 | ||
| C. | a、c极上都发生氧化反应 | D. | 甲中铁棒比乙中铁棒更易腐蚀 |
2.下列关于胶体的认识,错误的是( )
| A. | 在溶有1molFe(OH)3胶粒的胶体中,含有多于NA个的Fe(OH)3分子 | |
| B. | 将一束强光通过淀粉溶液,也能产生丁达尔效应 | |
| C. | “雨后彩虹”“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的知识有关 | |
| D. | 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体 |
3.设NA为阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 含16g氧原子的二氧化硅晶体中含有的δ键数目为2NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 12克石墨中含有的共价键数目为1.5NA | |
| D. | 2molSO2和1molO2在一定条件下反应所得混合气体分子数等于2 NA |