题目内容
16.下列各组中两个变化所发生的反应,属于同一类型的是( )①由乙烯、氢气制取乙烷、由乙烷、溴(气体)制溴乙烷
②乙烯使溴水褪色、乙炔使酸性高锰酸钾水溶液褪色
③由乙醇、乙酸制乙酸乙酯、由甘氨酸制得二肽
④由乙烯、氯化氢制取氯乙烷、由乙炔、氯化氢制取氯乙烯.
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
分析 ①由乙烯、氢气制取乙烷为加成反应、由乙烷、溴(气体)制溴乙烷为取代反应;
②乙烯使溴水褪色发生加成反应、乙炔使酸性高锰酸钾水溶液褪色发生氧化反应;
③由乙醇、乙酸制乙酸乙酯为取代反应、由甘氨酸制得二肽为取代反应;
④由乙烯、氯化氢制取氯乙烷为加成反应、由乙炔、氯化氢制取氯乙烯为加成反应.
解答 解:①由乙烯、氢气制取乙烷为加成反应、由乙烷、溴(气体)制溴乙烷为取代反应,反应类型不同,故不选;
②乙烯使溴水褪色发生加成反应、乙炔使酸性高锰酸钾水溶液褪色发生氧化反应,反应类型不同,故不选;
③由乙醇、乙酸制乙酸乙酯为取代反应、由甘氨酸制得二肽为取代反应,反应类型相同,故选;
④由乙烯、氯化氢制取氯乙烷为加成反应、由乙炔、氯化氢制取氯乙烯为加成反应,反应类型相同,故选;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应等为解答的关键,侧重有机反应类型的判断及分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.在10℃和4105Pa条件下,当反应aA(g)?dD(g)+eE(g)达到平衡后,维持温度不变,改变压强,容积可变,测得D的浓度变化如下:
(1)压强从4105Pa增加到6105Pa时,平衡向逆反应方向移动(填:正、逆),a<d+e(填:大于、小于、等于).
(2)压强从10105Pa增加到20105Pa时,平衡向正(填正、逆)反应方向移动,此时平衡中E状态不能为气体(填:不能、能);a>d(填:大于、小于、等于).
| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
(2)压强从10105Pa增加到20105Pa时,平衡向正(填正、逆)反应方向移动,此时平衡中E状态不能为气体(填:不能、能);a>d(填:大于、小于、等于).
7.1L 0.1mol/L的AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是( )
| A. | 电解质AgNO3溶液的浓度变为0.08mol/L | |
| B. | 阳极上产生112mLO2(标况) | |
| C. | 转移1.204×1022个电子 | |
| D. | 反应中有0.01mol的Ag被氧化 |
4.将500mL pH=5的硫酸铜溶液(足量)用惰性电极电解一段时间,溶液pH变为2,若使溶液的浓度、pH与电解前相同,可采取的方法是( )
| A. | 向溶液中加入0.245g Cu(OH)2 | B. | 向溶液中加入0.31gCuCO3 | ||
| C. | 向溶液中加入0.0025 molH2SO4 | D. | 向溶液中加入0.2gCuO |
1.利用如图所示装置(电极均为惰性电极) 可吸收SO2,并制取硫酸和烧碱溶液,下列说法正确的是( )

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
5.下列说法不正确的是( )
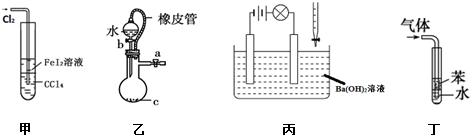

| A. | 甲装置可以用于比较Fe3+、I2、Cl2的氧化性强弱 | |
| B. | 乙装置中打开分液漏斗活塞,水不能顺利流下,说明该装置气密性良好 | |
| C. | 丙装置中若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 | |
| D. | 丁装置不能用于吸收HCl气体及防倒吸 |
6.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | NaHS水解:HS-+H2O?S2-+H3O+ | |
| C. | 在碱性介质中,氢氧燃料电池的负极反应式为:O2+4e-═2O2- | |
| D. | NaHCO3电离:NaHCO3?Na++HCO3- |