题目内容
4.填空题(1)浓H2SO4能够用于干燥某些气体,是由于它具有吸水性;下列气体能用浓硫酸来进行干燥的是①③(可多选,但只要有选错项,即得0分)
①Cl2 ②H2S ③CO2 ④NH3
(2)浓H2SO4能使纸片变黑,是由于它具有脱水性;
(3)浓H2SO4可以与Cu反应,是由于它具有强氧化性和酸性,化学学方程式是:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
分析 (1)浓H2SO4具有吸水性能够用于干燥某些气体,但浓硫酸又有强氧化性和酸性,则强还原性、碱性气体不能用浓硫酸干燥;
(2)浓H2SO4具有脱水性使纸片炭化变黑;
(3)浓H2SO4可以与Cu反应生成硫酸铜、二氧化硫和水,体现了浓硫酸的强氧化性和酸性.
解答 解:(1)浓H2SO4具有吸水性能够用于干燥某些气体,但浓硫酸又有强氧化性和酸性,则H2S具有强还原性,NH3具有碱性不能用浓硫酸干燥,故答案为:吸水;①③;
(2)浓H2SO4具有脱水性使纸片炭化变黑,故答案为:脱水;
(3)浓H2SO4可以与Cu反应生成硫酸铜、二氧化硫和水,方程式为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O,体现了浓硫酸的强氧化性和酸性,故答案为:酸;Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O.
点评 本题考查了浓H2SO4的性质,明确浓H2SO4的吸水性、脱水性、强氧化性是解本题关键,再结合基本概念来分析解答,题目难度不大.

练习册系列答案
相关题目
14.下列说法正确的是( )
| A. | 甲烷与氯气取代反应的产物二氯代甲烷无同分异构体说明甲烷是正四面体结构 | |
| B. | 等物质的量的乙烷与乙酸完全燃烧消耗氧气的量相等 | |
| C. | 按系统命名法,化合物 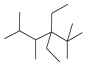 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| D. | 结构简式为 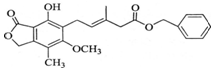 的化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 的化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
15.下列各组有机物只用水就鉴别的是( )
| A. | 乙醇、苯、硝基苯 | B. | 苯、己烷、溴苯 | C. | 苯、乙酸、己烯 | D. | 苯、乙醇、乙酸 |
12.已知镓和铝在周期表中位于同一纵行,氮化镓可把手机信号扩大10倍,让电脑的速度提高1万倍,将CD缩减到1英寸,下列有关氮化镓的说法中正确的是( )
| A. | 氮化镓是由主族元素与副族元素形成的化合物 | |
| B. | 镓元素比铝元素金属性弱 | |
| C. | 氮化镓中氮元素显+3价 | |
| D. | 氮原子最外层比镓原子最外层多2个电子 |
19.碱金属是典型的活泼金属,其根本原因是( )
| A. | 碱金属原子最外电子层上都只有1个电子,容易失去 | |
| B. | 碱金属在常温下易被氧化 | |
| C. | 碱金属单质的密度小,熔点和沸点低 | |
| D. | 碱金属原子的核电荷数比较小 |
9.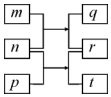 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径的大小W>X>Y | B. | 元素的非金属性Z>X>Y | ||
| C. | X的氢化物常温常压下为液态 | D. | Y的最高价氧化物的水化物为弱酸 |
13.0.1mol•L-1K2CO3溶液中下列表达式不正确的是( )
| A. | c(K+)>c(CO32-)>c(OH-)>c (HCO3-)>c(H+) | |
| B. | c(K+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol•L-1 | |
| D. | c(OH-)═c(H+)+2c(H2CO3)+c(HCO3-) |
9.苯是一种重要的有机化工原料,广泛用于合成橡胶、塑料和医药等方面.下列关于苯的叙述正确的是( )
| A. | 分子式为C6H6 | B. | 属于不饱和烃 | C. | 能在空气中燃烧 | D. | 无色无毒的液体 |