题目内容
3.下列叙述中,指定粒子的数目约为6.02×1023的是( )| A. | 1.6gCH4中含有的分子数 | |
| B. | 1molH2SO4中含有的H+ 数 | |
| C. | 2.4gMg中含有的原子数 | |
| D. | 标准状况下22.4LCO气体中含有的分子数 |
分析 A.依据n=$\frac{m}{M}$质量转化为物质的量;
B.1molH2SO4中含有2mol的氢离子;
C.依据n=$\frac{m}{M}$质量转化为物质的量;
D.依据n=$\frac{V}{{V}_{m}}$计算.
解答 解:A.1.6 g CH4物质的量为$\frac{1.6g}{16g/mol}$=0.1mol,含有6.02×1022个分子,故A错误;
B.根1molH2SO4中含有2mol的氢离子,氢离子数目为1.204×1024,故B错误;
C.2.4gMg物质的量为$\frac{2.4g}{24g/mol}$=0.1mol,含有的原子数,6.02×1022个,故C错误;
D.标准状况下,22.4LCO气体物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,含有的分子数6.02×1023,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关问题,注意物质与微粒的关系,明确好以物质的量为中心的各化学量与阿伏加德罗常数的关系为解答关键,题目较简单.

练习册系列答案
相关题目
11.医用酒精的浓度是( )
| A. | 25% | B. | 50% | C. | 75% | D. | 95% |
8.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是( )
| 选项 | 反应类型 | 反应条件 |
| A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
| B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
| C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
| D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
| A. | A | B. | B | C. | C | D. | D |
15.下列各组离子在强酸性无色透明溶液中能大量共存的是( )
| A. | Ba2+、Fe2+、Cl-、NO3- | B. | CO32-、SO42-、Na+、K+ | ||
| C. | Cl-、MnO4-、OH-、K+ | D. | Mg2+、SO42-、NO3-、Na+ |
12.下列说法中正确的是( )
| A. | l mol任何气体的体积都约是22.4L | |
| B. | l mol任何物质在标准状况下所占体积都约是22.4L | |
| C. | 不同的气体,体积相同,它们所含的分子数可能不同 | |
| D. | 在同温同压下,相同质量的氯气和氢气体积相同 |
13.在CuSO4、Fe2(SO4)3和ZnSO4混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是( )
| A. | 滤液中一定有Fe2(SO4)3和FeSO4 | |
| B. | 滤液中可能有CuSO4,一定有FeSO4、ZnSO4 | |
| C. | 滤渣中一定有Cu和Fe,一定无Zn | |
| D. | 滤渣中可能有Cu、Fe和Zn |
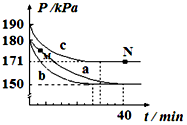 臭氧是理想的烟气脱硝试剂,原理为:2NO2(g)+O3(g)?N2O5(g)+O2(g).若在容积为10L的密闭容器中进行该反应,起始时充入0.4molNO2、0.2molO3,反应分别在a、b、c三种不同条件下进行,反应体系总压强随时间的变化如图所示.
臭氧是理想的烟气脱硝试剂,原理为:2NO2(g)+O3(g)?N2O5(g)+O2(g).若在容积为10L的密闭容器中进行该反应,起始时充入0.4molNO2、0.2molO3,反应分别在a、b、c三种不同条件下进行,反应体系总压强随时间的变化如图所示.