题目内容
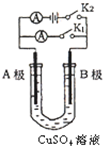 如图所示,U形管内盛有100mL的CuSO4溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的CuSO4溶液,按要求回答下列问题:(1)若A极材料是为Zn,B极材料是为石墨,打开K2,合上K1,则A极为
(2)若A、B极材料都为石墨,打开K1,合上K2.反应一段时间后,若忽略溶液的体积变化和气体的溶解,A、B两极收集到气体的体积(标准状况下)都为560mL,则原CuSO4溶液的物质的量浓度为
(3)如要用电解方法精炼粗铜,则A、B电极都要更换,其中A的材料应换成
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)该装置是原电池,较活泼的金属作负极,溶液中阳离子向正极移动,阴离子向负极移动.
(2)根据电解池的工作原理以及两极反应的电极反应式结合电子守恒来计算即可;
(3)电解精炼铜时,粗铜是阳极,纯铜是阴极,电解质溶液是含有铜离子的盐溶液.
(2)根据电解池的工作原理以及两极反应的电极反应式结合电子守恒来计算即可;
(3)电解精炼铜时,粗铜是阳极,纯铜是阴极,电解质溶液是含有铜离子的盐溶液.
解答:
解:(1)该装置是原电池,锌作负极,碳作正极,原电池放电时,溶液中阳离子向正极移动,阴离子向负极移动,所以溶液中氢氧根离子和硫酸根离子向A极移动.
故答案为:负;A;
(2)若A、B极材料都为石墨,打开K1,合上K2,构成电解池,A极是阴极,Cu2++2e-=Cu,2H++2e-=H2,B极是阳极,4OH--4e-=O2↑+2H2O,A、B两极收集到气体的体积(标准状况下)都为560mL即0.025mol,此时阳极上电子转移0.1mol,阴极上生成氢气转移电子是0.05mol,所以铜离子共得到0.05mol电子,铜离子的物质的量是0.025mol,所以原CuSO4溶液的物质的量浓度c=
=
=0.25mol/L,故答案为:0.25;
(3)用电解方法精炼粗铜,粗铜是阳极,纯铜是阴极,即A的材料应换成纯铜(或铜),在阳极上是金属锌铁镍等金属先失电子,在阴极上始终是铜离子得电子,所以电解后铜离子浓度会减小,故答案为:纯铜(或铜);减小.
故答案为:负;A;
(2)若A、B极材料都为石墨,打开K1,合上K2,构成电解池,A极是阴极,Cu2++2e-=Cu,2H++2e-=H2,B极是阳极,4OH--4e-=O2↑+2H2O,A、B两极收集到气体的体积(标准状况下)都为560mL即0.025mol,此时阳极上电子转移0.1mol,阴极上生成氢气转移电子是0.05mol,所以铜离子共得到0.05mol电子,铜离子的物质的量是0.025mol,所以原CuSO4溶液的物质的量浓度c=
| n |
| V |
| 0.025mol |
| 0.1L |
(3)用电解方法精炼粗铜,粗铜是阳极,纯铜是阴极,即A的材料应换成纯铜(或铜),在阳极上是金属锌铁镍等金属先失电子,在阴极上始终是铜离子得电子,所以电解后铜离子浓度会减小,故答案为:纯铜(或铜);减小.
点评:本题涉及原电池和电解池的工作原理知识,注意知识的归纳和整理是解题的关键,难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目