题目内容
在下列各溶液中,离子一定能大量共存的是( )
| A、强酸性溶液中:K+、Al3+、CH3COO-、SO42- | ||
B、水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO
| ||
| C、室温下,pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl- | ||
| D、室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.强酸性溶液中含大量的H+;
B.水电离出来的c(H+)=10-13mol/L的溶液,为酸或碱溶液;
D.pH=1的无色溶液,显酸性,且离子均为无色;
D.室温下,pH=1的溶液,显酸性,离子之间发生氧化还原反应.
B.水电离出来的c(H+)=10-13mol/L的溶液,为酸或碱溶液;
D.pH=1的无色溶液,显酸性,且离子均为无色;
D.室温下,pH=1的溶液,显酸性,离子之间发生氧化还原反应.
解答:
解:A.强酸性溶液中含大量的H+,与CH3COO-结合生成弱电解质,不能大量共存,故A错误;
B.水电离出来的c(H+)=10-13mol/L的溶液,为酸或碱溶液,HCO3-既能与酸又能与碱反应,一定不能共存,故B错误;
D.pH=1的无色溶液,显酸性,该组离子之间不反应,能大量共存,且离子均为无色,故C正确;
D.室温下,pH=1的溶液,显酸性,H+、Fe2+、NO3-离子之间发生氧化还原反应,不能大量共存,故D错误;
故选C.
B.水电离出来的c(H+)=10-13mol/L的溶液,为酸或碱溶液,HCO3-既能与酸又能与碱反应,一定不能共存,故B错误;
D.pH=1的无色溶液,显酸性,该组离子之间不反应,能大量共存,且离子均为无色,故C正确;
D.室温下,pH=1的溶液,显酸性,H+、Fe2+、NO3-离子之间发生氧化还原反应,不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的考查,题目难度不大.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、铝片跟氢氧化钠溶液反应:Al+2OH-+2H2O=AlO2-+H2↑ |
| B、醋酸铵溶液和盐酸反应:CH3COONH4+H+=CH3COOH+NH4+ |
| C、向乙醇中加入金属钠:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
 已知某温度时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )
已知某温度时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )| A、a点表示溶液中c(CH3COO-)约为10-3 mol/L | ||
| B、b点表示的溶液中c(Na+)>c(CH3COO-) | ||
| C、c点表示CH3COOH和NaOH恰好反应完全 | ||
D、d点表示的溶液中
|
对下列各溶液进行电解,通电一段时间后,溶液颜色不会发生显著改变的是( )
| A、以石墨为电极,电解含甲基橙的0.01mol/L H2SO4溶液 |
| B、以铜为电极,电解1mol/L H2SO4溶液 |
| C、以石墨为电极,电解含酚酞的饱和NaCl溶液 |
| D、以石墨为电极,电解1mol/L的KBr溶液 |
下列离子方程式不正确的是( )
| A、将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ |
| B、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| C、醋酸钠的水解:CH3COO-+H3O+?CH3COOH+H2O |
D、苯酚钠溶液中通入CO2气体: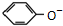 +CO2+H2O→ +CO2+H2O→ +HCO3- +HCO3- |
下列实验装置图合理的是( )
A、 如图装置可用于证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 |
B、 如图装置能构成锌铜原电池 |
C、 如图装置可用于粗铜的电解精炼 |
D、 如图装置可用于在实验室测定中和反应的反应热 |
下列各组离子在溶液中能大量共存的是( )
| A、K+、Na+、SO42-、CO32- |
| B、NH4+、Na+、SO42-、OH- |
| C、H+、K+、HCO3-、Cl- |
| D、Al3+、K+、OH-、NO3- |
