题目内容
14.已知下列热化学方程式:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8kJ•mol-13Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
则14g CO气体与足量FeO充分反应得到Fe单质和CO2气体时的释放或吸收的热量为( )
| A. | 放出218 kJ | B. | 放出109kJ | C. | 吸收218 kJ | D. | 吸收109 kJ1 |
分析 由盖斯定律可知,反应CO+FeO═Fe+CO2可由$\frac{①×3-(②+③×2)}{6}$得到,以此来计算反应热.
解答 解:①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g);△H=-24.8kJ/mol,
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1,
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g);△H=+640.4kJ/mol,
由盖斯定律可知,$\frac{①×3-(②+③×2)}{6}$得到反应$\frac{1}{2}$CO(g)+$\frac{1}{2}$FeO(s)═$\frac{1}{2}$Fe(s)+$\frac{1}{2}$CO2(g),△H=$\frac{24.8×3-(-47.2)-640.5×2}{6}$KJ/mol=-109kJ/mol,
故选:B.
点评 本题考查学生利用盖斯定律计算反应热,熟悉已知反应与目标反应的关系是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
4.下列装置能达到实验目的是( )
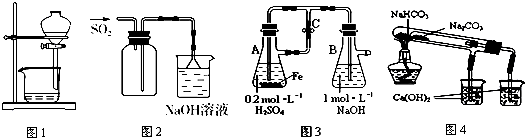

| A. | 图1用于放出碘的苯溶液 | |
| B. | 图2用于实验室收集SO2 | |
| C. | 图3用于实验室制备Fe(OH)2 | |
| D. | 图4用于比较NaHCO3和Na2CO3热稳定性 |
5. 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂 1mol N-N键吸收193kJ热量,断裂 1mol N≡N键吸收941kJ热量,则下列说法不正确的是( )
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂 1mol N-N键吸收193kJ热量,断裂 1mol N≡N键吸收941kJ热量,则下列说法不正确的是( )
 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂 1mol N-N键吸收193kJ热量,断裂 1mol N≡N键吸收941kJ热量,则下列说法不正确的是( )
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂 1mol N-N键吸收193kJ热量,断裂 1mol N≡N键吸收941kJ热量,则下列说法不正确的是( )| A. | N4与N2互为同素异形体 | |
| B. | 1 mol N4气体转化为N2时要放出724 kJ能量 | |
| C. | N4变成N2是化学变化 | |
| D. | N4不可能是分子晶体 |
9.下列各组物质的反应,一定属于氧化还原反应的是( )
| A. | 金属和酸 | B. | 盐和碱 | C. | 盐和酸 | D. | 酸和碱 |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 过氧化钠与水反应时,生成2.24L氧气转移的电子数为0.2NA | |
| B. | 1L 0.1mol•L-1的NaHS溶液中HS-和S2-离子数之和为0.1NA | |
| C. | 标准状况下,2.24L三氯甲烷分子中含有共价键总数为0.4NA | |
| D. | 15g${\;}_{\;}^{14}{C}_{\;}^{16}O$和15g${\;}_{\;}^{12}{C}_{\;}^{18}O$中含有的中子数均为8NA |
6.下列说法不正确的是( )
| A. | 互为手性异构体的分子互为镜像 | |
| B. | 熔点:SiCl4<MgCl2<SiO2 | |
| C. | 水加热到很高的温度都很难以分解,是因为水中含有氢键 | |
| D. | 断裂化学键的过程不一定发生化学变化 |