题目内容
15.某有机物的结构简式如图,有关说法正确的是( )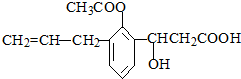
| A. | 该物质共有两种含氧官能团 | |
| B. | 该物质属于芳香烃 | |
| C. | 1 mol该有机物能与3mol的NaOH反应 | |
| D. | 1 mol该有机物在一定条件下可以消耗6molH2 |
分析 由结构可知,分子中含碳碳双键、-COOC-、-OH、-COOH,结合烯烃、酯、醇、羧酸的性质来解答.
解答 解:A.含-COOC-、-OH、-COOH三种含氧官能团,故A错误;
B.含O元素,为烃的衍生物,故B错误;
C.-COOC-、-COOH及-COOC-水解生成的酚-OH均与NaOH反应,则1 mol该有机物能与3mol的NaOH反应,故C正确;
D.只有苯环与碳碳双键与氢气发生加成反应,则1 mol该有机物在一定条件下可以消耗4molH2,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、酯、醇、羧酸的性质,题目难度不大.

练习册系列答案
相关题目
5.在光照条件下,将等物质的量的甲烷和氯气充分反应,所得产物中物质的量最多的是( )
| A. | CH3Cl | B. | CH2Cl | C. | CHCl3 | D. | HCl |
6.在一定温度下的恒容的密闭容器中,当下列物理量不再发生变化时,可逆反应H2(g)+I2(g)═2HI(g)达到平衡状态的是( )
| A. | 混合气体的压强恒定不变 | |
| B. | 混合气体的密度不再改变 | |
| C. | H2、I2、HI的浓度相等 | |
| D. | I2在混合气体中的体积分数不再改变 |
3.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 含有离子键的化合物一定是离子化合物 | |
| C. | 由共价键形成的物质一定是共价化合物 | |
| D. | 非金属原子间形成的化学键一定是共价键 |
10.核内中子数为N的R2+离子,质量数为A,则ng它的氧化物中所含质子的物质的是( )
| A. | $\frac{n}{16+A}$(A-N+8)mol | B. | $\frac{n}{16+A}$(A-N+10)mol | C. | (A-N+2)mol | D. | $\frac{n}{A}$(A-N+6)mol |
20.下列分子式只表示一种纯净物的是( )
| A. | C2H6O | B. | C3H6 | C. | C2H4 | D. | C5H12 |
7.化学能可与热能、电能等相互转化.下列表述不正确的是( )


| A. | 化学反应中能量变化的主要原因是化学键的断裂与形成 | |
| B. | 中和反应中,反应物的总能量比生成物的总能量高 | |
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图II所示的反应为放热反应 |
5.下列关于卤素的说法正确的是( )
| A. | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到上层液体呈紫色 | |
| B. | 液溴有强挥发性,保存时应加少量水液封 | |
| C. | Cl2可以从NaBr水溶液中置换出溴单质,可类推F2可以从NaCl水溶液中置换出氯单质 | |
| D. | HX的还原性顺序为:HF>HCl>HBr>HI |