题目内容
3.苯分子实际上不具有碳碳单键和碳碳双键的简交替结构,下面是某同学收集的有关事实,其中可以作为证据的有( )①苯的间位二元取代物只有一种;②苯的邻位二元取代物只有一种;③苯不能使酸性KMnO4溶液褪色;④苯不能与溴水反应.
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | 全部 |
分析 ①无论苯的结构中是否有碳碳双键和碳碳单键,苯的间位二元取代物都无同分异构体;
②苯的结构中若存在单双键交替结构,苯的邻位二元取代物有两种;
③苯不能使酸性高锰酸钾溶液褪色,证明苯分子中不存在碳碳双键;
④苯不能使溴水褪色,证明苯分子中不存在碳碳双键.
解答 解:①无论苯的结构中是否有碳碳双键和碳碳单键,苯的间位二元取代物都无同分异构体,所以不能说明苯不是单双键交替结构,故①错误;
②若苯的结构中存在单双键交替结构,苯的邻位二元取代物有两种,但实际上苯的邻位二元取代物只有一种,说明苯不是单双键交替结构,故②正确;
③苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,可以证明苯环结构中不存在C-C单键与C=C双键的交替结构,故③正确;
④苯不能与溴水反应,证明苯分子中不存在碳碳双键,从而可证明苯不具有碳碳单键和碳碳双键的简交替结构,故④正确;
故选B.
点评 本题考查苯的结构与性质,题目难度不大,明确苯的组成、结构与性质为解答关键,注意熟练掌握判断苯分子中不存在碳碳单键和碳碳双键的简交替结构的方法,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
14.下列是卤素单质(F2、Cl2、Br2、I2)的沸点与相对分子质量的关系图,下列说法错误的是( )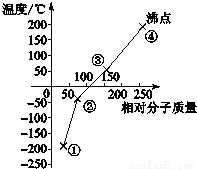

| A. | 单质①是最活泼的非金属单质 | |
| B. | 单质②能使品红溶液褪色 | |
| C. | 保存少量的单质③时加少量水进行水封 | |
| D. | 单质④的氢化物在卤素氢化物中沸点最高 |
11.能用键能知识加以解释的是( )
| A. | 稀有气体的化学性质很不活泼 | B. | H2O的沸点比H2S高 | ||
| C. | 干冰易升华 | D. | 氮气的化学性质很稳定 |
18.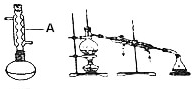 苯佐卡因(对氨基甲酸乙酯)常用于创面、溃疡面及痔疮的止痛,也是镇咳药退咳药的中间体,有关数据和实验装置图如下:
苯佐卡因(对氨基甲酸乙酯)常用于创面、溃疡面及痔疮的止痛,也是镇咳药退咳药的中间体,有关数据和实验装置图如下:
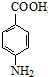 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$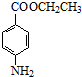 +H2O.
+H2O.
合成反应:
在圆底烧瓶中加入0.4g(0.0029mol)对氨基苯甲酸和0.082mol乙醇,振荡溶解,将烧瓶置于冰水浴并加入0.22mL浓硫酸(0.004mol),将反应混合物在水浴上加热回流1h,并不时振荡.
分离提纯:
冷却后,分批加入10%的NaHCO3溶液直至无明显气泡产生,再加少量NaCHO3溶液至pH≈9,转移至分液漏斗中,用乙醚分两次萃取,并向乙醚层加入无水硫酸钠,得到乙醚层,冷却结晶,最终得到产物0.2g.
(1)仪器A的名称:球形冷凝管,烧瓶置于水浴中的原因反应温度低于水的沸点,受热均匀,偏于控制温度,.
(2)加热前还需在烧瓶中加入碎瓷片.
(3)在合成反应中,圆底烧瓶的容积最合适的是A
A.10mL B.20mL C.50mL
(4)分液漏斗使用前必须进行的操作是查漏,乙醚层位于上层(填“上层”或“下层”);分离提纯操作加入无水硫酸钠的作用是吸收乙醚中的水.
(5)合成反应中加入过量乙醇的目的是提高对氨基苯甲酸的利用率;分离提纯过程中10%NaHCO3溶液的作用是除去混有对氨基苯甲酸.
(6)本实验中苯佐卡因的产率为41.8%(结果保留三位有效数字)
 苯佐卡因(对氨基甲酸乙酯)常用于创面、溃疡面及痔疮的止痛,也是镇咳药退咳药的中间体,有关数据和实验装置图如下:
苯佐卡因(对氨基甲酸乙酯)常用于创面、溃疡面及痔疮的止痛,也是镇咳药退咳药的中间体,有关数据和实验装置图如下: +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.| 相对分子质量 | 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | 水中溶解性 | |
| 乙醇 | 46 | 0.789 | -117.3 | 78.5 | 与水任意比互溶 |
| 对氨基苯甲酸 | 137 | 1.374 | 188 | 339.9 | 微溶于水 |
| 对氨基苯甲酸乙酯 | 165 | 1.039 | 90 | 172 | 难溶于水,易溶于醇、醛类 |
在圆底烧瓶中加入0.4g(0.0029mol)对氨基苯甲酸和0.082mol乙醇,振荡溶解,将烧瓶置于冰水浴并加入0.22mL浓硫酸(0.004mol),将反应混合物在水浴上加热回流1h,并不时振荡.
分离提纯:
冷却后,分批加入10%的NaHCO3溶液直至无明显气泡产生,再加少量NaCHO3溶液至pH≈9,转移至分液漏斗中,用乙醚分两次萃取,并向乙醚层加入无水硫酸钠,得到乙醚层,冷却结晶,最终得到产物0.2g.
(1)仪器A的名称:球形冷凝管,烧瓶置于水浴中的原因反应温度低于水的沸点,受热均匀,偏于控制温度,.
(2)加热前还需在烧瓶中加入碎瓷片.
(3)在合成反应中,圆底烧瓶的容积最合适的是A
A.10mL B.20mL C.50mL
(4)分液漏斗使用前必须进行的操作是查漏,乙醚层位于上层(填“上层”或“下层”);分离提纯操作加入无水硫酸钠的作用是吸收乙醚中的水.
(5)合成反应中加入过量乙醇的目的是提高对氨基苯甲酸的利用率;分离提纯过程中10%NaHCO3溶液的作用是除去混有对氨基苯甲酸.
(6)本实验中苯佐卡因的产率为41.8%(结果保留三位有效数字)
8.下列说法错误的是( )
| A. | 二氧化碳和环氧丙烷在催化作用下可生成一种可降解的高聚物,可减少二氧化碳对环境的影响 | |
| B. | 化石燃料的燃烧和含硫金属矿石的冶炼等都是造成SO2污染的重要原因 | |
| C. | 氟氯烃的大量使用会破坏臭氧层,火箭、导弹将大量废气排放到高空,也会加速臭氧分解 | |
| D. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 |
2.(1)已知Na2S2O3+H2SO4═Na2SO4+S↓+SO2+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究浓度对化学反应速率的影响,应选择①②或③④.(填实验编号);探究温度对化学反应速率的影响,应选择①④.(填实验编号).
(2)甲同学设计如图实验流程探究Na2S2O3的化学性质.
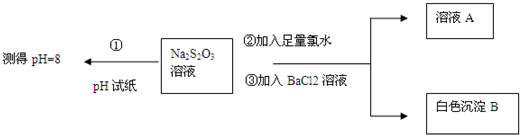
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和还原 性.
(Ⅱ)生成白色沉淀B的离子方程式是SO42-+Ba2+=BaSO4↓.
(Ⅲ)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
(2)甲同学设计如图实验流程探究Na2S2O3的化学性质.

(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和还原 性.
(Ⅱ)生成白色沉淀B的离子方程式是SO42-+Ba2+=BaSO4↓.
(Ⅲ)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
3.下列说法正确的是( )
| A. | Cl2、Br2、I2的熔沸点依次升高 | |
| B. | 因为自然界中没有游离态的P元素,所以非金属性P>N | |
| C. | 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,一定无K+ | |
| D. | 已知FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变程度相同 |
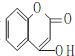 )的路线如下图所示:
)的路线如下图所示: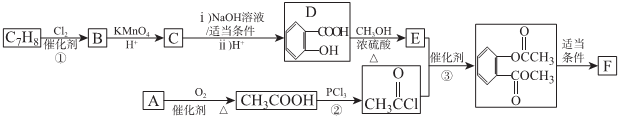
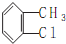 .
.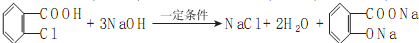 .
.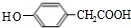 .
.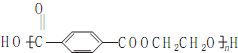 ),参照A→乙酸的表示方法,写出相应的合成路线图
),参照A→乙酸的表示方法,写出相应的合成路线图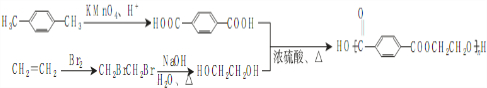 .
.