题目内容
20.紫杉醇(paclitaxel)是一种抗癌药,化合物D是紫杉醇的侧链,D的合成路线如下: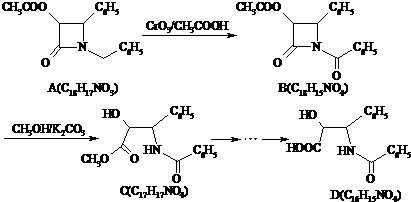
(1)A的合成应用了2010年诺贝尔化学奖的获奖成果--交叉偶联反应,反应式如下(已配平):
CH3COOCH2COCl+X$\stackrel{交叉偶联}{→}$ A+HCl
X分子中含碳氮双键(C=N),其结构简式为
 .
.(2)已知酯和酰胺在过量醇中能发生醇解反应:
CH3COOC2H5+CH3OH$\stackrel{一定条件}{→}$ CH3COOCH3+C2H5OH
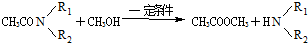
“醇解反应”的反应类型为取代反应,B转化为C中另一产物的结构简式为CH3COOCH3.
(3)若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F.
①E在一定条件下能发生缩聚反应,写出所得高分子化合物的一种可能的结构简式:
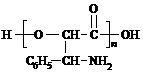 或
或 ;
;②F的同分异构体中,属于芳香族化合物、能发生银镜反应且核磁共振氢谱有4个峰的有两种,请写出其中一种的结构简式:
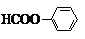 或
或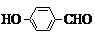 .
.(4)已知:①RCHO$→_{H+}^{HCN}$
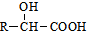 ②R′COOH$\stackrel{PCI_{3}}{→}$R′COCl
②R′COOH$\stackrel{PCI_{3}}{→}$R′COCl写出以甲醛和乙醛为原料合成CH3COOCH2COCl的路线流程图(无机试剂任选).合成路线流程图示例如下:
CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
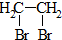
分析 (1)根据原子守恒,及A与CH3COOCH2COCl的结构,确定X的结构简式.
(2)根据酯和酰胺的结构以及生成的酯的结构分析解答;
由酰胺在过量醇中能发生醇解反应的信息可知,在如图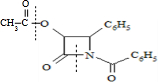 所示虚线发生化学键断裂,O原子、N原子连接甲醇中羟基中的H原子,-OCH3连接断键处的C原子;
所示虚线发生化学键断裂,O原子、N原子连接甲醇中羟基中的H原子,-OCH3连接断键处的C原子;
(3)最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F,由D的结构可知,E为HOOC-CH(OH)-CH(NH2)-C6H5,F为C6H5-COOH,
①E分子中含有-COOH、-OH、-NH2,可以通过形成酯缩聚生成高聚物,也可以通过成肽键发生缩聚反应生成高聚物;
②C6H5-COOH的同分异构体中,属于芳香族化合物、能发生银镜反应,故含有苯环、醛基或是甲酸酚酯,核磁共振氢谱有4个峰,含有4种不同的H原子,据此书写;
(4)CH3COOCH2COCl中含有酯基,结合信息可知,先由CH3CHO氧化生成CH3COOH,HCHO在HCN、酸性条件下合成HOCH2COOH,HOCH2COOH在PCl3条件下合成HOCH2COCl,再由CH3COOH与HOCH2COCl在浓硫酸、加热条件下发生酯化反应生成CH3COOCH2COCl.
解答 解:(1)CH3COOCH2COCl+X→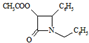 +HCl,X分子中含碳氮双键(C=N),应在如图
+HCl,X分子中含碳氮双键(C=N),应在如图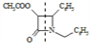 虚线所示位置是反应成键位置,故X为
虚线所示位置是反应成键位置,故X为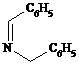
故答案为: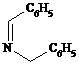
(2)由反应方程式CH3COOC2H5+CH3OH$\stackrel{一定条件下}{→}$CH3COOCH3+C2H5OH,可知-OCH3取代-OC2H5,
CH3CO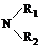
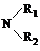
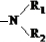 ,故酯和酰胺在过量醇中能发生醇解反应属于取代反应,由酰胺在过量醇中能发生醇解反应的信息可知,在如图
,故酯和酰胺在过量醇中能发生醇解反应属于取代反应,由酰胺在过量醇中能发生醇解反应的信息可知,在如图 所示虚线发生化学键断裂,O原子、N原子连接甲醇中羟基中的H原子,-OCH3连接断键处的C原子,故还生成CH3COOCH3,
所示虚线发生化学键断裂,O原子、N原子连接甲醇中羟基中的H原子,-OCH3连接断键处的C原子,故还生成CH3COOCH3,
故答案为:取代反应;CH3COOCH3;
(3)最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F,由D的结构可知,E为HOOC-CH(OH)-CH(NH2)-C6H5,F为C6H5-COOH,
①E分子中含有-COOH、-OH、-NH2,可以通过形成酯缩聚生成高聚物,也可以通过成肽键发生缩聚反应生成高聚物,故可能的高聚物为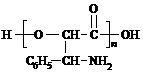

故答案为: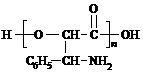

②C6H5-COOH的同分异构体中,属于芳香族化合物、能发生银镜反应,故含有苯环、醛基或是甲酸酚酯,核磁共振氢谱有4个峰,含有4种不同的H原子,符合条件的结构为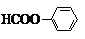
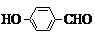
故答案为: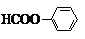
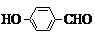
(4)CH3COOCH2COCl中含有酯基,结合信息可知,先由CH3CHO氧化生成CH3COOH,HCHO在HCN、酸性条件下合成HOCH2COOH
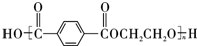
,HOCH2COOH在PCl3条件下合成HOCH2COCl,再由CH3COOH与HOCH2COCl在浓硫酸、加热条件下发生酯化反应生成CH3COOCH2COCl,故合成路线流程: ,
,
故答案为: .
.
点评 本题考查有机物合成,为高频考点,根据反应前后有机物结构简式变化确定反应类型,难点是有机合成路线设计,要根据反应物、产物及其结构特点结合题给信息设计,注意基础知识的灵活运用,侧重考查学生综合知识运用能力,题目难度中等.

 口算题天天练系列答案
口算题天天练系列答案| A. | NaH的电子式为Na+[:H]- | |
| B. | NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 | |
| C. | 微粒半径H-<Li+ | |
| D. | NaH与H2O反应时,水作氧化剂 |
| A. | 含H+的溶液一定呈酸性 | |
| B. | pH=7的溶液一定呈中性 | |
| C. | c(OH-)═c(H+)的溶液一定呈中性 | |
| D. | 水中加入硫酸恢复至室温后,Kw=c(H+)•c(OH-)将变大 |
| A. | 胶体和溶液具有相同的性质:均一、稳定,静置后不产生沉淀 | |
| B. | 布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分 | |
| C. | 可以利用丁达尔效应区分胶体和溶液 | |
| D. | 只有胶状的物质如胶水、果冻类的才能称为胶体 |
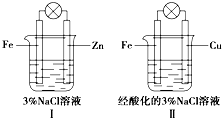
| A. | Ⅰ和Ⅱ中正极均被保护 | |
| B. | Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ | |
| C. | Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- | |
| D. | Ⅰ和Ⅱ中灯泡均会发亮 |
 电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)X的电极名称是阴极.
(2)若X、Y都是惰性电极,a是硝酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,Y极上的电极反应式为2H2O-4e-=4H++O2↑,一段时间后,在X极附近观察到的现象是有气泡,溶液变红.
(3)若X、Y都是惰性电极,a是足量的AgNO3溶液,写出电解过程的化学方程式4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3 ,电解一段时间,当电极上通过的电子为0.2mol时,阴极上生成物的质量为21.5g.
(4)若要用电镀方法在铁表面镀一层金属铜,应该选择的方案是D.
| 方案 | X | Y | a溶液 |
| A | 铜 | 石墨 | CuSO4 |
| B | 铜 | 铁 | CuSO4 |
| C | 铁 | 铜 | Fe(NO3)3 |
| D | 铁 | 铜 | CuSO4 |

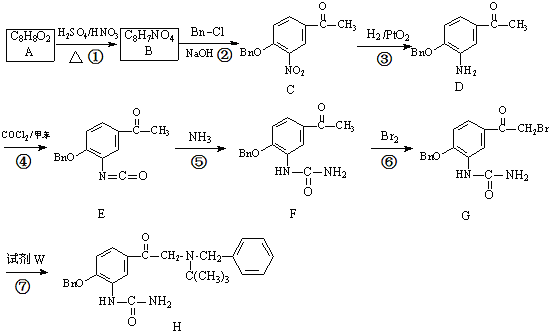
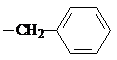 试剂W
试剂W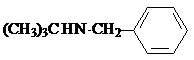 .
.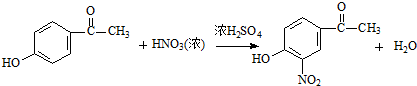 .
.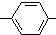 CH2
CH2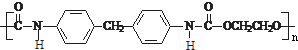 .
.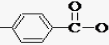 -CH2CH2N(C2H5)2(无机试剂任用)
-CH2CH2N(C2H5)2(无机试剂任用) 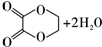 ,B的结构简式为OGC-CHO.
,B的结构简式为OGC-CHO.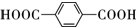
 .
. .
.