题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、标准状况下,28g氮气所含有的原子数目为NA |
| B、常温常压下,44.8L氯化氢气体所含的分子数为2NA |
| C、标准状况下,22.4L水中含有NA个水分子 |
| D、化学反应中,1mol金属镁变成镁离子时失去的电子数目为2NA |
考点:阿伏加德罗常数
专题:
分析:A.计算时分清氮气是双原子分子;
B.依据气体摩尔体积的条件应用分析,标准状况气体摩尔体积为22.4L/mol;
C.标准状况水不是气体;
D.镁容易失去最外层2个电子变为镁离子.
B.依据气体摩尔体积的条件应用分析,标准状况气体摩尔体积为22.4L/mol;
C.标准状况水不是气体;
D.镁容易失去最外层2个电子变为镁离子.
解答:
解:A.28g氮气物质的量为1mol,1molN2所含原子数为2N,故A错误;
B.依据气体摩尔体积的条件应用分析,标准状况气体摩尔体积为22.4L/mol,44.8L氯化氢气体物质的量不是2mol,故B错误;
C.标准状况水不是气体,22.4L水不是1mol,故C错误;
D.镁容易失去最外层2个电子变为镁离子,则化学反应中1mol金属镁变成镁离子时失去2mol电子,电子数目为2NA,故D正确.
故选D.
B.依据气体摩尔体积的条件应用分析,标准状况气体摩尔体积为22.4L/mol,44.8L氯化氢气体物质的量不是2mol,故B错误;
C.标准状况水不是气体,22.4L水不是1mol,故C错误;
D.镁容易失去最外层2个电子变为镁离子,则化学反应中1mol金属镁变成镁离子时失去2mol电子,电子数目为2NA,故D正确.
故选D.
点评:本题考查有关阿伏伽德罗常数的计算,明确标况下物质的状态、气体摩尔体积、物质的构成、原子的最外层电子等即可解答,难度不大.

练习册系列答案
相关题目
常温下,不跟单质硅起反应的物质是( )
| A、氢氧化钠溶液 | B、氢氟酸 |
| C、浓硝酸 | D、氟气 |
设nA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A、7 g CnH2n中含氢原子数为nA | ||||
| B、4.6 g N2O4、NO2混合气体中含有中子数为2.3nA | ||||
C、在反应5NH4NO3
| ||||
| D、电解精炼铜时每转移nA个电子,阳极溶解32 g铜 |
下列各组离子,在pH>7的溶液中能量共存,且溶液为无色透明的离子组是( )
| A、K+、MnO4-、Cl-、SO42- |
| B、Na+、NO3-、CO32-、Cl- |
| C、Na+、H+、NO3-、SO42- |
| D、Ca2+、NO3-、CO32-、Cl- |
下列反应中,不是氧化还原反应的是( )
A、H2+Cl2
| ||||
| B、Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||||
C、2H2O
| ||||
| D、Zn+2HCl═ZnCl2+H2↑ |
含Ba(OH)2l mol的稀溶液与足量稀盐酸反应,放出114.6kJ的热量,表示该反应中和热的热化学方程式正确的是( )
| A、Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l);△H=-114.6kJ/mol | ||||
| B、Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l);△H=+114.6kJ/mol | ||||
C、
| ||||
D、
|
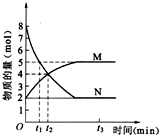 化学反应速率与化学平衡的理论研究对工农业生产有重要的意义.一定温度下,在容积为20L的密闭容器中进行a N(g)?b M(g) 的化学反应,M、N 的物质的量随时间的变化曲线如图所示:
化学反应速率与化学平衡的理论研究对工农业生产有重要的意义.一定温度下,在容积为20L的密闭容器中进行a N(g)?b M(g) 的化学反应,M、N 的物质的量随时间的变化曲线如图所示: