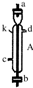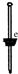题目内容
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液480mL.根据这两种溶液的配制情况回答下列问题:
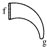
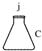
(1)如图所示的仪器中配制溶液需要的是 (填字号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称).

(2)根据计算用托盘天平称取NaOH.若NaOH溶液在转移至容量瓶时,洒落了少许,则需要如何操作: .
(3)根据计算得知,所需质量分数为98%、密度为l.84g/cm3的浓硫酸的体积为 ml.
(4)下列操作会使配制的NaOH溶液浓度偏低的是 .
A.用滤纸称量NaOH
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡.
(1)如图所示的仪器中配制溶液需要的是

(2)根据计算用托盘天平称取NaOH.若NaOH溶液在转移至容量瓶时,洒落了少许,则需要如何操作:
(3)根据计算得知,所需质量分数为98%、密度为l.84g/cm3的浓硫酸的体积为
(4)下列操作会使配制的NaOH溶液浓度偏低的是
A.用滤纸称量NaOH
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据配制一定物质的量浓度溶液用到仪器选择;
(2)洒落了少许,溶质氢氧化钠的物质的量减少,需要重新配置;
(3)根据c=
计算浓硫酸的浓度,再根据浓硫酸稀释前后溶质的物质的量不变计算;
(4)依据C=
进行误差分析,凡是能够使n增大,或者使V减小的操作,都会使C偏大;凡是能够使n减小,V增大的操作都会使C偏小.
(2)洒落了少许,溶质氢氧化钠的物质的量减少,需要重新配置;
(3)根据c=
| 1000ρω |
| M |
(4)依据C=
| n |
| V |
解答:
解:(1)配制一定物质的量浓度溶液用到仪器:托盘天平、量筒、500mL容量瓶、烧杯、玻璃棒、胶头滴管、药匙等;
故答案为:BDE;烧杯和玻璃棒;
(2)若NaOH溶液在转移至容量瓶时,洒落了少许,溶质氢氧化钠的物质的量减少,需要重新配置,否则所配溶液浓度偏小,故答案为:重新配置;
(3)质量分数为98%、密度为1.84g/cm3的浓硫酸的浓度为:c=
=1000×98%×1.84g/ml98g/mol=18.4mol/L,浓硫酸稀释前后溶质的物质的量不变,设浓硫酸的体积为V,所以18.4mol/L×V=0.5/L×0.5L,得V=0.0136L=13.6ml,故答案为:13.6;
(4)A.用滤纸称量NaOH,氢氧化钠容易吸收空气的水和二氧化碳,称取的氢氧化钠的质量减少,n偏小,则浓度偏小,故A正确;
B.选用的容量瓶内有少量蒸馏水,对溶液的体积不会产生影响,所配溶液准确,故B错误;
C.定容摇匀后,液面下降,又加水至刻度线,相当于多加了水,溶液的体积偏大,浓度偏小,故C正确;
D.整个配制过程中,容量瓶不振荡,溶质与水分子不能充分接触,使溶液的体积偏小,浓度偏大,故D错误;
故选:AC.
故答案为:BDE;烧杯和玻璃棒;
(2)若NaOH溶液在转移至容量瓶时,洒落了少许,溶质氢氧化钠的物质的量减少,需要重新配置,否则所配溶液浓度偏小,故答案为:重新配置;
(3)质量分数为98%、密度为1.84g/cm3的浓硫酸的浓度为:c=
| 1000ρω |
| M |
(4)A.用滤纸称量NaOH,氢氧化钠容易吸收空气的水和二氧化碳,称取的氢氧化钠的质量减少,n偏小,则浓度偏小,故A正确;
B.选用的容量瓶内有少量蒸馏水,对溶液的体积不会产生影响,所配溶液准确,故B错误;
C.定容摇匀后,液面下降,又加水至刻度线,相当于多加了水,溶液的体积偏大,浓度偏小,故C正确;
D.整个配制过程中,容量瓶不振荡,溶质与水分子不能充分接触,使溶液的体积偏小,浓度偏大,故D错误;
故选:AC.
点评:本题考查了一定物质的量浓度溶液的配置,熟悉配置一定物质的量浓度溶液的步骤和所用药品是解题关键,注意依据C=
进行误差分析,题目难度中等.
| n |
| V |

练习册系列答案
相关题目
标准状况下的28L NH3溶于125mL水中,若所得氨水的密度近似为1g?cm-3,则下列说法正确的是( )
A、物质的量浓度(mol?L-1)与溶液质量分数、密度(g?cm-3)的关系为:c=
| ||
| B、此氨水中NH3的物质的量浓度近似为9.9 mol?L-1 | ||
| C、此氨水中NH3的物质的量浓度近似为8.55 mol?L-1 | ||
| D、此氨水中NH3的质量分数为0.17 |
实验室需要配制2mol/l的NaCl溶液450ml,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A、450ml,52.65g |
| B、任意规格,52.65g |
| C、500 ml,58.5g |
| D、1000 ml,117g |
下列说法正确的是( )
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
| A、①②③④⑤ | B、② |
| C、①③④⑤ | D、①②⑤ |
一定温度下,对于反应N2+O2?2NO在密闭容器中进行,下列措施能加快反应速率的是( )
| A、改变温度 |
| B、恒容,充入N2 |
| C、恒容,充入He气 |
| D、恒压,充入He气 |