题目内容
向0.5L FeCl3和AlCl3的混合溶液中加入amol NaOH时,产生的沉淀量可达最大值,继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到bmol时,沉淀量不再减少,求原溶液中Fe3+的物质的量浓度.
考点:有关混合物反应的计算
专题:计算题
分析:产生的沉淀量达最大值,发生反应:AlCl3+3NaOH=Al(OH)3↓+3NaCl、FeCl3+3NaOH=Fe(OH)3↓+3NaCl,此时消耗amolNaOH,继续加入NaOH溶液,沉淀开始溶解,发生反应:Al(OH)3+NaOH=NaAlO2+2H2O,该阶段消耗氢氧化钠为(b-a)mol,根据方程式计算沉淀量最大时氢氧化铝的物质的量,进而计算生成氢氧化铝消耗的n(NaOH)、氯化铝的物质的量,再计算与FeCl3溶液反应氢氧化钠的物质的量,根据方程式计算c(FeCl3),以此解答.
解答:
解:溶解氢氧化铝消耗NaOH为(b-a)mol,则:
Al(OH)3+NaOH=NaAlO2+2H2O
1mol 1mol
(b-a)mol (b-a)mol
由AlCl3+3NaOH=Al(OH)3↓+3NaCl,可知氯化铝消耗NaOH为:3(b-a)mol,n(AlCl3)=(b-a)mol,
则发生反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,消耗氢氧化钠为amol-3(b-a)mol=(4a-3b)mol,故所以n(FeCl3)=
×(4a-3b)mol=
mol,
故原溶液中c(Fe3+)=
=
mol/L,
答:原溶液中Fe3+的物质的量浓度为
mol/L.
Al(OH)3+NaOH=NaAlO2+2H2O
1mol 1mol
(b-a)mol (b-a)mol
由AlCl3+3NaOH=Al(OH)3↓+3NaCl,可知氯化铝消耗NaOH为:3(b-a)mol,n(AlCl3)=(b-a)mol,
则发生反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,消耗氢氧化钠为amol-3(b-a)mol=(4a-3b)mol,故所以n(FeCl3)=
| 1 |
| 3 |
| 4a-3b |
| 3 |
故原溶液中c(Fe3+)=
| ||
| 0.5L |
| 4a-6b |
| 3 |
答:原溶液中Fe3+的物质的量浓度为
| 4a-6b |
| 3 |
点评:本题考查化学方程式的有关计算,为高频考点,侧重学生的分析能力和计算能力的考查,难度不大,清楚发生的反应是关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质中属于混合物的是( )
①五水硫酸铜 ②液氧 ③干冰 ④稀盐酸 ⑤氢氧化铁胶体 ⑥乙醇⑦洁净的矿泉水.
①五水硫酸铜 ②液氧 ③干冰 ④稀盐酸 ⑤氢氧化铁胶体 ⑥乙醇⑦洁净的矿泉水.
| A、①②⑤⑦ | B、④⑤⑦ |
| C、③④⑥ | D、⑤⑥⑦ |
不能用排空气法收集的气体是( )
| A、02 |
| B、NH3 |
| C、H2 |
| D、NO |
已知H2SO3+I2+H2O→2HI+H2SO4.向NaBr、NaI、Na2SO3混合液中,通入一定量氯气,将溶液蒸干并充分燃烧,得到固体剩余物质的组成可能是( )
| A、NaCl、Na2SO4 |
| B、NaCl、NaBr、Na2SO4 |
| C、NaCl、Na2SO4、I2 |
| D、NaCl、NaI、Na2SO4 |
下列关于有机物的认识正确的是( )
| A、C2H6与氯气发生取代反应、C2H4与HCl发生加成反应均可得到纯净的C2H5Cl |
| B、将甲烷和乙烯的混合气体通过盛有浓溴水的洗气瓶,即可提纯甲烷 |
| C、乙烯结构中含有碳碳双键,苯中不含有碳碳双键,但两者均可以发生加成反应 |
| D、苯使酸性KMn04溶液、溴水都褪色,发生的都是氧化反应 |
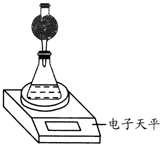 某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol?L-1 HNO3、2.00mol?L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.
某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol?L-1 HNO3、2.00mol?L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.