题目内容
用化学方程式解释下列问题:
(1)盛放烧碱液的试剂瓶不能用玻璃塞
(2)用NaOH溶液除去铝表面的保护层 、
(3)制备氢氧化亚铁需隔绝空气
(4)从氧化还原反应的角度看,在制备H2、CO2、Cl2三种气体时,盐酸作还原剂 .
(5)6种物质:N2O、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O可以组成一个已配平的化学方程式: .
(1)盛放烧碱液的试剂瓶不能用玻璃塞
(2)用NaOH溶液除去铝表面的保护层
(3)制备氢氧化亚铁需隔绝空气
(4)从氧化还原反应的角度看,在制备H2、CO2、Cl2三种气体时,盐酸作还原剂
(5)6种物质:N2O、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O可以组成一个已配平的化学方程式:
考点:化学方程式的书写,氧化还原反应,硅和二氧化硅
专题:化学用语专题,氧化还原反应专题
分析:(1)玻璃中的SiO2与NaOH反应,生成具有粘性的Na2SiO3,会粘住瓶塞;
(2)铝在空气中和氧气反应生成氧化铝薄膜,氧化铝属于两性氧化物和碱反应生成盐和水;
(3)氢氧化亚铁易被空气中的氧气氧化为氢氧化铁;
(4)利用Zn+2HCl═ZnCl2+H2↑、CaCO3+2HCl═CaCl2+CO2↑+H2O、MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O反应及元素的化合价变化分析;
(5)元素处于最高价只有氧化性,元素居于低价有还原性,根据所给物质的化合价情况来分析配平.
(2)铝在空气中和氧气反应生成氧化铝薄膜,氧化铝属于两性氧化物和碱反应生成盐和水;
(3)氢氧化亚铁易被空气中的氧气氧化为氢氧化铁;
(4)利用Zn+2HCl═ZnCl2+H2↑、CaCO3+2HCl═CaCl2+CO2↑+H2O、MnO2+4HCl (浓)
| ||
(5)元素处于最高价只有氧化性,元素居于低价有还原性,根据所给物质的化合价情况来分析配平.
解答:
解:(1)玻璃中的SiO2与NaOH反应,生成具有粘性的Na2SiO3,会粘住瓶塞,其反应为SiO2+2NaOH═Na2SiO3+H2O,
故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(2)铝在空气中和氧气反应生成氧化铝薄膜,反应的化学方程式是:4Al+3O2═2Al2O3,氧化铝和碱反应:Al2O3+2NaOH═2NaAlO2+H2O,
故答案为:4Al+3O2═2Al2O3;Al2O3+2NaOH═2NaAlO2+H2O;
(3)新制氢氧化亚铁在空气被氧化,氢氧化亚铁被氧化成氢氧化铁,反应的化学方程式是为:4Fe(OH)2+2H2O+O2═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(4)由Zn+2HCl═ZnCl2+H2↑可知,HCl中H元素的化合价降低,体现HCl的氧化性,作氧化剂;
由CaCO3+2HCl═CaCl2+CO2↑+H2O可知,没有元素的化合价变化,生成盐,体现HCl的酸性,作酸;
由MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O可知,生成盐,体现其酸性,生成氯气时Cl元素的化合价升高,体现HCl的还原性,作还原剂,
故答案为:MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O;
(5)所给的物质组合中,HNO3中氮元素化合价位于最高价,具有氧化性,对应还原产物为N2O,能将还原性的FeSO4氧化为Fe2(SO4)3,根据氢原子守恒,水在生成物中,配平后发生的反应为:30HNO3+24FeSO4=8Fe(NO3)3+8Fe2(SO4)3+3N2O+15H2O,
故答案为:24FeSO4+30HNO3═8Fe(NO3)3+8 Fe2(SO4)3+3N2O↑+15H2O.
故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(2)铝在空气中和氧气反应生成氧化铝薄膜,反应的化学方程式是:4Al+3O2═2Al2O3,氧化铝和碱反应:Al2O3+2NaOH═2NaAlO2+H2O,
故答案为:4Al+3O2═2Al2O3;Al2O3+2NaOH═2NaAlO2+H2O;
(3)新制氢氧化亚铁在空气被氧化,氢氧化亚铁被氧化成氢氧化铁,反应的化学方程式是为:4Fe(OH)2+2H2O+O2═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(4)由Zn+2HCl═ZnCl2+H2↑可知,HCl中H元素的化合价降低,体现HCl的氧化性,作氧化剂;
由CaCO3+2HCl═CaCl2+CO2↑+H2O可知,没有元素的化合价变化,生成盐,体现HCl的酸性,作酸;
由MnO2+4HCl (浓)
| ||
故答案为:MnO2+4HCl (浓)
| ||
(5)所给的物质组合中,HNO3中氮元素化合价位于最高价,具有氧化性,对应还原产物为N2O,能将还原性的FeSO4氧化为Fe2(SO4)3,根据氢原子守恒,水在生成物中,配平后发生的反应为:30HNO3+24FeSO4=8Fe(NO3)3+8Fe2(SO4)3+3N2O+15H2O,
故答案为:24FeSO4+30HNO3═8Fe(NO3)3+8 Fe2(SO4)3+3N2O↑+15H2O.
点评:本题考查学生根据反应原理书写化学方程式的能力,明确发生的化学反应是解答本题的关键,注意化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,题目难度不大.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、麦芽糖及其水解产物均能发生银镜反应 |
| B、用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
D、用甘氨酸(H2N-CH2-COOH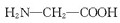 )和丙氨酸( )和丙氨酸(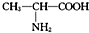 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
物质的量均为0.4mol的 Na、Mg、Al 分别与150ml 浓度为2mol/L的盐酸反应,相同温度和压强下比较产生H2的体积 ( )
| A、Na产生的多 |
| B、Mg产生的多 |
| C、Al产生的多 |
| D、一样多 |
下列说法中,正确的是( )
| A、△H>0表示放热反应,△H<0 表示吸热反应 |
| B、若反应△H>0;△S<0,则反应一定能自发进行 |
| C、1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
| D、热化学方程式中的化学计量数表示物质的量,所以可以是分数 |
下列离子方程式正确的是( )
| A、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| B、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| C、过量二氧化硫通入氢氧化钠溶液中:SO2+OH-═SO32-+H2O |
| D、氢氧化铝与足量盐酸反应,Al(OH)3+3H+═Al3++3H2O |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+
O2(g)=CO2(g)+2H2(g);△H=-192.9kJ/mol
下列说法错误的是( )
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+
| 1 |
| 2 |
下列说法错误的是( )
| A、1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ | ||
B、根据反应①和②推知反应:H2(g)+
| ||
| C、CH3OH转变成H2的过程不一定要吸收能量 | ||
D、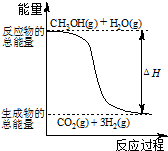 反应①中的能量变化如图所示 |