题目内容
(14分)
X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+3、+5、+7,核电荷数按照Z、X、Y、W的顺序增大。已知Z的原子次外层的电子数为2,W、X原子次外层电子数为8。
(1)请写出元素Y的原子结构示意图: ;其中元素W在周期表中的位置: 。
(2)用电子式表示X与W形成化合物的过程: 。
(3)X、Y、Z、W的原子半径由大到小的顺序为: 。(用元素符号表示)
(4)请写出W的单质与X的最高价氧化物对应水化物反应的化学方程式:
。
(5)元素X与元素Y相比,金属性较强的是 (用元素符号表示),请举一例实验事实证明这一结论:
【答案】
(1) ;第三周期、ⅦA族
;第三周期、ⅦA族
(2)
(3)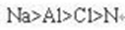
(4)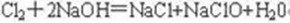
(5)Na,钠与水反应比铝要剧烈
【解析】

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )
| X | Y |
| Z | W |
| A、若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数) |
| B、若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱 |
| C、若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸 |
| D、若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应 |





