题目内容
写出下列反应的方程式:(第一个方程式需用双线桥法标出电子转移的方向和数目)
(1)工业制漂白粉的原理 ;
(2)过氧化钠与二氧化碳 .
(1)工业制漂白粉的原理
(2)过氧化钠与二氧化碳
考点:化学方程式的书写
专题:
分析:(1)氯气和石灰乳反应生成氯化钙和次氯酸钙;氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目;
(2)过氧化钠与二氧化碳反应生成碳酸钠和氧气.
(2)过氧化钠与二氧化碳反应生成碳酸钠和氧气.
解答:
解:(1)氯气和石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,氯气中氯元素从0价变为CaCl2中-1价氯和Ca(ClO)2中+1价氯,所以用双线桥标出电子转移的方向和数目为: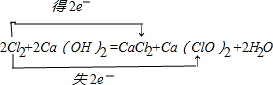 ,
,
故答案为: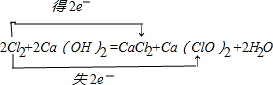 ;
;
(2)过氧化钠与二氧化碳反应生成碳酸钠和氧气,方程式为:2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2.
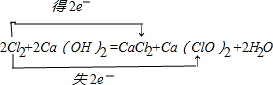 ,
,故答案为:
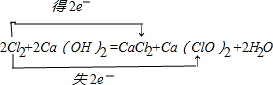 ;
;(2)过氧化钠与二氧化碳反应生成碳酸钠和氧气,方程式为:2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2.
点评:本题考查氧化还原反应的特征和实质以及化学方程式的书写知识,把握、氯气、过氧化钠的性质以及反应的化学方程式的书写方法及注意事项是解题关键,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
下列物质中,属于电解质的是( )
| A、蔗糖 | B、盐酸 |
| C、氯化钠 | D、二氧化碳 |
下列说法正确的是( )
| A、二氧化碳分子中存在共价键和分子间作用力 |
| B、甲烷、氨和水都是由极性键结合而成的极性分子 |
| C、同主族不同元素的最高价氧化物,一定具有相同的晶体结构 |
| D、氟化氢的沸点高于氯化氢的沸点,正丁烷的沸点高于异丁烷的沸点 |
2.3g钠放入100g水中,所得溶液的质量分数是( )
| A、等于2.3% |
| B、大于2.3% |
| C、等于4% |
| D、大于4% |
下列反应的离子方程式书写正确的是( )
| A、钠和水反应 Na+H2O═Na++OH-+H2↑ |
| B、Cl2与KBr溶液反应 Cl2+2Br-═2Cl-+Br2 |
| C、氯气与NaOH溶液反应 Cl2+OH-═Cl-+ClO-+H2O |
| D、盐酸与石灰石反应 CO32-+2H+═CO2↑+H2O |