题目内容
13.现有34.0g NH3,试计算(写出计算过程)(1)气体的物质的量2mol.
(2)在标准状况下的体积44.8L.
(3)分子数目2NA.
分析 M(NH3)=17g/mol,结合n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$计算相关物理量.
解答 解:(1)n=$\frac{34.0g}{17g/mol}$=2mol,故答案为:2mol;
(2)V=2mol×22.4L/mol=44.8L,故答案为:44.8L;
(3)n=2mol,则N=2NA,故答案为:2NA.
点评 本题考查物质的量的相关计算,为高频考点,侧重考查学生的分析能力和计算能力,题目较为基础,注意把握公式的运用.

练习册系列答案
相关题目
12.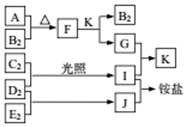 如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )
如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )
 如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )
如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )| A. | B氢化物的沸点高于其同主族其它元素氢化物的沸点 | |
| B. | 原子半径大小:A>C>B>E>D | |
| C. | F中既含有离子键又含有极性共价键 | |
| D. | G中的阴离子能抑制水的电离 |
4.下列说法不正确的是( )
| A. | 明矾可作自来水的净水剂 | B. | 氢氧化铝可作胃酸的中和剂 | ||
| C. | 二氧化碳可用作钠着火的灭火剂 | D. | 小苏打可作面包的发泡剂 |
1.下列物质的转化在给定条件下能实现的是( )
| A. | Na $\stackrel{O_{2}/△}{→}$Na2O2 $\stackrel{HI(aq)}{→}$NaI | |
| B. | Fe2O3$\stackrel{H_{2}SO_{4}(aq)}{→}$Fe2(SO4)3(aq)$\stackrel{△}{→}$无水Fe2(SO4)3 | |
| C. | H2SiO3 $\stackrel{△}{→}$SiO2 $\stackrel{HCl(aq)}{→}$SiCl4 | |
| D. | 粗铜Cu$\stackrel{盐酸}{→}$CuCl2(aq)$\stackrel{电解}{→}$Cu |
8.下列反应中属于氧化还原反应,但水既不做氧化剂,又不做还原剂的是( )
| A. | ICl+H2O=HCl+HIO | B. | 2K+2H2O=2KOH+H2↑ | ||
| C. | 2F2+2H2O=4HF+O2 | D. | 2Na2O2+2H2O=4NaOH+O2 |
5.一种元素与另一种元素的本质区别是( )
| A. | 相对原子质量不同 | B. | 质子数不同 | ||
| C. | 中子数不同 | D. | 电子数不同 |
2.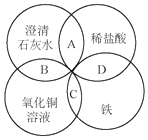 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )| A. | OH-+HCl═H2O+Cl- | B. | Ca(OH)2+Cu2+═Ca2++Cu(OH)2 | ||
| C. | Fe+Cu2+═Cu+Fe2+ | D. | Fe+2H+═Fe3++2H2↑ |
10.下列实验操作正确的是( )
| A. | 分液时,先将上层液体从上口倒出 | |
| B. | 萃取时,振荡后,须打开活塞放气 | |
| C. | 蒸馏时,先点燃酒精灯,后通冷凝水 | |
| D. | 蒸发时,将溶剂蒸干一段时间后,熄灭酒精灯 |