题目内容
11.过氧化钠(化学式为Na2O2)可用在呼吸面具中作为氧气来源.Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.以下是某兴趣小组进行的探究活动.(1)利用如下图所示实验装置制取氧气,请回答有关问题.

①实验室制取CO2的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
②表明CO2未被Na2O2完全吸收的实验现象为澄清石灰水变浑浊.
③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的氧气密度比空气的大,氧气有助燃性性质.
④若A装置产生的CO2中混有水蒸气,要检验干燥的CO2能否与Na2O2反应生成O2,以上实验装置应如何改进在A、B装置之间增加气体干燥装置
(2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验.
①有同学猜想X可能是酸、碱或盐中的一种.通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是Na2O2和CO2都不含氢元素,根据质量守恒定律,二者反应后不可能生成含氢元素的酸或碱.
②同学们通过讨论和实验证明了X是Na2CO3.以下是他们设计的有关Na2CO3性质的探究实验,将下表填写完整.
| 实验操作 | 现 象 | 有关的化学方程式 |
| 实验一:取少量固体样品,滴加稀盐酸,然后将产生的气体通入澄清石灰水 | 有气泡产生 澄清石灰水变浑浊 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O |
| 实验二:取少量固体样品, 加水配成溶液,滴加适量的氯化钙或 氯化钡等 溶液 | 有白色沉淀产生 | Na2CO3+CaCl2=CaCO3↓+2NaCl或 Na2CO3+BaCl2=BaCO3↓+2NaCl等 |
分析 (1)①实验室用大理石和稀盐酸制备CO2,其反应为CaCO3+2HCl═CaCl2+H2O+CO2↑;
②装置C中的澄清石灰水就是检验CO2是否反应完全,如果CO2没有反应完全,则C中的澄清石灰水变浑浊;
③D装置长进短处是向上排空气的方法,因为氧气的密度比空气大,所以采用向上排空气法收集气体,氧气能使带火星的木条复燃,是因为氧气具有助燃性;
④因为制出的CO2带有水,所以要在A、B之间加一个干燥装置;
(2)①因为反应物是Na2O2和CO2,因此在产物中不可能有H元素出现,而酸或碱中都含有H元素,所以X不可能是酸或碱.②根据反应方程式可知,是盐酸与碳酸钠反应,盐酸与碳酸钠反应的现象是产生气泡.根据碳酸钠的性质可知,碳酸钠与钙盐或钡盐反应会产生白色沉淀;
(3)解:设生成氧气的质量为x,生成氢氧化钠的质量为y.
2Na2O2+2H2O=4NaOH+O2↑
156 160 32
7.8g y x
X=1.6g
Y=8g
氢氧化钠溶液中溶质的质量分数为:
8g/40g×100%=20%
答:氢氧化钠溶液中溶质的质量分数为20%.
解答 解:(1)①实验室用大理石和稀盐酸制备CO2,其反应为CaCO3+2HCl═CaCl2+H2O+CO2↑,故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②装置C中的澄清石灰水就是检验CO2是否反应完全,如果CO2没有反应完全,则C中的澄清石灰水变浑浊,故答案为:澄清石灰水变浑浊;
③D装置长进短处是向上排空气的方法,因为氧气的密度比空气大,所以采用向上排空气法收集气体,氧气能使带火星的木条复燃,是因为氧气具有助燃性,故答案为:氧气密度比空气的大,氧气有助燃性;
④因为制出的CO2带有水,所以要在A、B之间加一个干燥装置,故答案为:在A、B装置之间增加气体干燥装置;
(2)①因为反应物是Na2O2和CO2,因此在产物中不可能有H元素出现,而酸或碱中都含有H元素,所以X不可能是酸或碱,故答案为:Na2O2和CO2都不含氢元素,根据质量守恒定律,二者反应后不可能生成含氢元素的酸或碱;
②②根据反应方程式可知,是盐酸与碳酸钠反应,盐酸与碳酸钠反应的现象是产生气泡.根据碳酸钠的性质可知,碳酸钠与钙盐或钡盐反应会产生白色沉淀,
故答案为:
| 实验操作 | 现 象 | 有关的化学方程式 |
| 滴加稀盐酸,然后将产生的气体通入澄清石灰水 | 有气泡产生 | |
| 氯化钙或 氯化钡等 | Na2CO3+CaCl2=CaCO3↓+2NaCl或 Na2CO3+BaCl2=BaCO3↓+2NaCl等 |
2Na2O2+2H2O=4NaOH+O2↑
156 160 32
7.8g y x
解之得:x=1.6g;y=8g
氢氧化钠溶液中溶质的质量分数为:
$\frac{8g}{40g}$×100%=20%
答:氢氧化钠溶液中溶质的质量分数为20%.
点评 这是一道综合性强的实验习题,既有实验装置的分析,又有物质性质的检验,还有溶液质量分数的计算,要想能准确解答这类习题,首先要会分析各仪器的作用,然后掌握各种物质的性质

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中的值$\frac{C{H}_{3}COOH}{C{H}_{3}CO{O}^{-}}$减小 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 再加入10mlpH=11的NaOH溶液,混合液pH=7 |
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能发生反应 | |
| C. | 反应物和生成物所具有的总能量决定了放热还是吸热 | |
| D. | 吸热反应只能在加热的条件下才能进行 |
 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:| 实验编号 | HA物质的量浓度 (mol•L-1) | NaOH物质的量浓度 (mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从第①组情况分析,混合溶液pH=9的原因是A-+H2O?HA+OH-(用离子方程式表示),该组所得混合溶液中由水电离出的c(OH-)=10-5mol•L-1.
(2)第②组情况表明,c>0.2(选填“>”、“<”或“=”),该混合液中离子浓度c(A-) 与c(Na+) 的大小关系是c(A-)=c(Na+).
(3)从第③组实验结果分析,说明此时HA的电离程度>NaA的水解程度(选填“>”、“<”或“=”),该混合溶液中各离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
(4)将一定浓度的NaA溶液稀释100倍时,其pH变化如图 A、B、C曲线中的B(填字母)曲线.
(5)由上述所涉及的溶质组成以下四组等体积溶液:
甲:0.1mol/LNaA
乙:0.1mol/LNaA和0.1mol/LHA
丙:0.1mol/LHA
丁:0.1mol/LNaA和0.1mol/LNaOH
则A-离子浓度由大到小的顺序为乙>丁>甲>丙(填序号).
| A. | 1 mol•L-1的醋酸溶液的c(H+)约为0.01 mol•L-1 | |
| B. | 醋酸能与NaHCO3溶液反应放出CO2 | |
| C. | 醋酸的导电性比盐酸溶液的弱 | |
| D. | 10 mL 1 mol•L-1醋酸恰好与10 mL1 mol•L-1NaOH溶液完全反应 |
| A. | 当a=5时,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) | |
| B. | 当a=10时,c(Cl-)+c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| C. | 当a=15时,c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.04 mol•L-1 | |
| D. | 当a=20时,c(Na+)=c(H+)>c(HC2O4-)>c(C2O42-) |
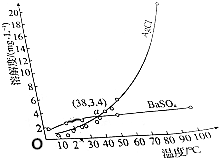
| A. | a点时,AgCl和BaSO4饱和溶液的密度基本相同 | |
| B. | AgCl的溶解是吸热过程 | |
| C. | 室温时,向等体积的饱和AgCl和BaSO4溶液中分别加入足量的浓BaCl2溶液,析出BaSO4沉淀的质量比AgCl多 | |
| D. | 可以用重结晶的方法分离AgCl和BaSO4 |
 苏教版《化学1》“活动与探究”:配制100mL 0.100mol•L-1 Na2CO3溶液.
苏教版《化学1》“活动与探究”:配制100mL 0.100mol•L-1 Na2CO3溶液.
 .
.