题目内容
下列说法正确的是
A.催化剂可以改变某反应的焓变
B.置换反应不一定是氧化还原反应
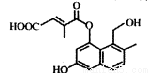
C.氨基酸溶液既显酸性又显碱性
D.催化剂不可能提高可逆反应中反应物的转化率
D
【解析】
试题分析:A.催化剂只改变反应速率和活化能的大小,无论是否加入催化剂,反应热都不变,A错误;B.置换反应有单质参加和生成,元素的化合价一定发生变化,一定是氧化还原反应,B错误;C.溶液的酸碱性取决于溶液中氢离子和氢氧根离子的浓度,氨基酸溶液的酸碱性是一定的,不可能既显酸性又显碱性,但氨基酸溶液既能与酸反应,又能与碱反应,C错误;D.催化剂不改变平衡移动,不可能提高可逆反应中反应物的转化率,D正确;选D。
考点:考查催化剂,氧化还原反应,氨基酸的性质等知识。

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目

 Si + 2CO↑
Si + 2CO↑