题目内容
(7分)
Q、W、X、Y、Z五种短周期元素,原子序数依次增大。Q在元素周期表中原子半径最小,W元素最高正价与最低负价代数和为0;Y与Q同主族;X、Z分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)X、Z简单离子半径较大是 (用离子符号表示)。
(2)由这五种元素中的若干种组成的化合物甲、乙、丙、丁在水溶液中有如下转化关系:
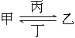
其中丙是溶于水显酸性的气体,丁是强碱。
①若乙常作为焙制糕点的发酵粉,则乙含有的化学键类型有 。
②若乙是难溶物,甲溶液与过量的丙生成乙的离子方程式为: 。
(7分)
(1)O2-(2分)
(2)①离子键、共价键(2分)填写一个得1分,只写离子或共价不得分,多写不给分。
②[Al(OH)4]- + CO2=Al(OH)3↓+ HCO3-(3分)
【解析】
试题分析:Q、W、X、Y、Z五种短周期元素,原子序数依次增大.Q在元素周期表中原子半径最小,则Q为H元素;X、Z分别是地壳中含量最高的非金属元素和金属元素,则X为O、Z为Al;Y与Q同主族,Y原子序数大于氧元素,则Y为Na元素;W元素最高正价与最低负价代数和为0,处于ⅣA族,结合原子序数可知,W为碳元素。
(1)O2-、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故离子半径O2->Al3+,故答案为:O2-
(2)上述五种元素中的若干种组成的化合物甲、乙、丙、丁,其中丙是溶于水显酸性的气体,丁是强碱,丙为CO2、丁为NaOH。①若乙常作为焙制糕点的发酵粉,则乙为NaHCO3,含有离子键、共价键。
②若乙是难溶物,则乙为Al(OH)3,甲是Na[Al(OH)4],甲与过量的CO2反应生成生成氢氧化铝沉淀与碳酸氢钠,反应离子方程式为:[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-。
考点:本题考查元素的推断、原子结构、元素周期律、方程式的书写、化学键。

 2HI(g),温度一定,在1L的密闭容器中加入2molH2(g)和1molI2(g)开始反应,2min末测知容器中生成了1.2mol HI(g),下列说法正确的是
2HI(g),温度一定,在1L的密闭容器中加入2molH2(g)和1molI2(g)开始反应,2min末测知容器中生成了1.2mol HI(g),下列说法正确的是
 X
X Y
Y Zn路径流动
Zn路径流动