题目内容
14.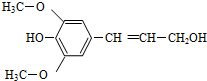 膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示.下列有关芥子醇的说法正确的是( )| A. | 芥子醇的分子式是C11H12O4 | |
| B. | 芥子醇分子中所有碳原子可能在同一平面 | |
| C. | 1mol芥子醇能与足量溴水反应消耗3molBr2 | |
| D. | 1mol芥子醇与足量的氢气反应消耗氢气4mol |
分析 该有机物中含有醚基、酚羟基、碳碳双键和醇羟基,具有醚、酚、烯烃和醇的性质,据此分析解答.
解答 解:A.该分子的分子式是C11H14O4,故A错误;
B.分子中含有苯环、乙烯等基础分子的共面结构,单键可以旋转,所有碳原子可能在同一平面,故B错误;
C.苯环上酚羟基邻对位不存在氢原子,只有碳碳双键和溴发生加成反应,所以1mol芥子醇能与足量溴水反应消耗1molBr2,故C错误;
D.苯环和碳碳双键都能和氢气发生加成反应,所以1mol芥子醇与足量的氢气反应消耗氢气4mol,故D正确;
故选D.
点评 本题考查物质结构和性质,明确物质官能团及其性质的关系是解本题关键,熟练掌握常见有机物官能团,难点是原子共面的判断,易错选项是B.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
4.下列说法正确的是( )
| A. | 分子式为C7H8O,且含苯环的有机化合物有4种 | |
| B. | 乙醇能使酸性高锰酸钾溶液褪色 | |
| C. | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的使酸性KMnO4溶液褪色的气体只是乙烯 | |
| D. | 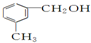 遇FeCl3溶液可显紫色 遇FeCl3溶液可显紫色 |
5.下列说法正确的是( )
| A. | 物质发生化学变化都伴随着能量变化 | |
| B. | 任何反应中的能量变化都表现为热量变化 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 所有化学反应都可以设计成原电池 |
2.(1)BrO3-+Cl2═Br2+2ClO3-(2)5Cl2+I2+6H2O═2HIO3+10HCl
(3)ClO3-+5Cl-+6H+═3Cl2+3H2O,由上述反应,判断氧化能力强弱,正确的是( )
(3)ClO3-+5Cl-+6H+═3Cl2+3H2O,由上述反应,判断氧化能力强弱,正确的是( )
| A. | ClO3->BrO3->IO3->Cl2 | B. | BrO3->Cl2>IO3->ClO3- | ||
| C. | BrO3->ClO3->Cl2>IO3- | D. | Cl2>BrO3->ClO3->IO3- |
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA | |
| B. | 4.2 g C3H6中含有的碳碳双键数一定为0.1 NA | |
| C. | 1 mol-OH中电子数为10 NA | |
| D. | 标准状况下,2.24 L CHCl3的原子总数为0.1 NA |
3.用聚光手电筒照射下列分散系,不能观察到丁达尔效应的是( )
| A. | KOH溶液 | B. | Fe(OH)3胶体 | C. | 雾 | D. | 鸡蛋清水溶液 |
4.为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和 A中加热装置已略).实验过程:
①检查装置气密性后,在各仪器中添加相应试剂.
②打开弹簧夹K1~K4,通入一段时间N2,将T型管插入B中,继续通入N2,然后关闭K1、K3、K4.
③打开活塞a,滴加一定量的浓盐酸,加热A.
④当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
⑤打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子.
⑥打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
⑦更换试管D,重复过程⑤,检验B溶液中的离子.
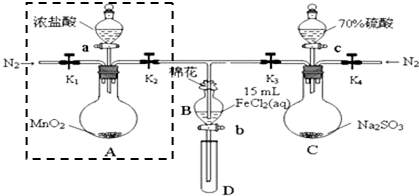
试回答下列问题:
(1)检验图中虚线框内装置气密性的具体操作是关闭K1、K2,打开分液漏斗的盖子和活塞,向其中加入水,一段时间后分液漏斗尖嘴处不再滴液即证明气密性良好.
(2)C中发生反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
(3)若将制取的SO2通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为2MnO4-+5SO2+4H2O=2Mn2++5SO42-+4H+.
(4)B中的棉花通常会浸润NaOH溶液试剂;实验②中通入N2的作用是排除装置中的空气,防止FeCl2溶液被O2氧化.
(5)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性 Cl2>Fe3+>SO2的是乙、丙(填“甲”、“乙”或“丙”).
(6)进行实验过程⑥时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色.
查阅资料:Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色)
提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色.某同学设计如下实验,证实该假设成立:
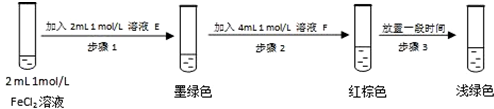
①溶液E和F分别为Na2SO3(或可溶性亚硫酸盐)、FeCl3.
②请结合方程式和化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因Fe3+与SO32-反应Fe3++SO32-=Fe2++SO42-,使c(SO32-)减小,平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色.
①检查装置气密性后,在各仪器中添加相应试剂.
②打开弹簧夹K1~K4,通入一段时间N2,将T型管插入B中,继续通入N2,然后关闭K1、K3、K4.
③打开活塞a,滴加一定量的浓盐酸,加热A.
④当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
⑤打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子.
⑥打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
⑦更换试管D,重复过程⑤,检验B溶液中的离子.

试回答下列问题:
(1)检验图中虚线框内装置气密性的具体操作是关闭K1、K2,打开分液漏斗的盖子和活塞,向其中加入水,一段时间后分液漏斗尖嘴处不再滴液即证明气密性良好.
(2)C中发生反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
(3)若将制取的SO2通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为2MnO4-+5SO2+4H2O=2Mn2++5SO42-+4H+.
(4)B中的棉花通常会浸润NaOH溶液试剂;实验②中通入N2的作用是排除装置中的空气,防止FeCl2溶液被O2氧化.
(5)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性 Cl2>Fe3+>SO2的是乙、丙(填“甲”、“乙”或“丙”).
| 过程⑤B溶液中含有的离子 | 过程⑦B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色)
提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色.某同学设计如下实验,证实该假设成立:

①溶液E和F分别为Na2SO3(或可溶性亚硫酸盐)、FeCl3.
②请结合方程式和化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因Fe3+与SO32-反应Fe3++SO32-=Fe2++SO42-,使c(SO32-)减小,平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色.
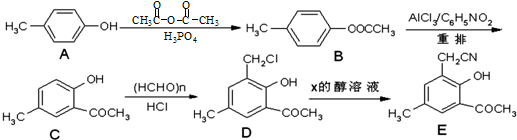
 (任写一种).
(任写一种). .
.