题目内容
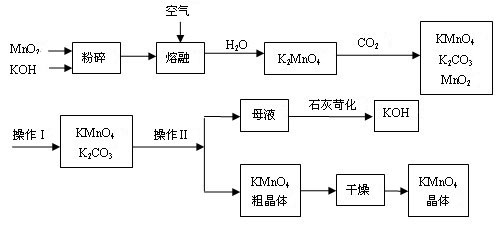
工业制备高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是____(填代号)。
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
(2)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是______(填代号)。
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
(3)上述流程中可以循环使用的物质有 . (写化学式)。
(4)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
(5)该生产中需要纯净的CO2气体。若实验室要制备纯净的CO2,所需试剂最好选择(选填代号) 。
a.石灰石 b.稀HCl c.稀H2SO4 d.纯碱
(6)操作Ⅰ的名称是 ;操作Ⅱ根据KMnO4和K2CO3两物质在 (填性质)上的差异,采用 (填操作步骤).趁热过滤得到KMnO4粗晶体。
(每空1分,共9分)
(1)ab
(2)d
(3)MnO2 ;KOH
(4)2/3
(5)cd
(6)过滤;溶解度;浓缩结晶
解析:KMnO4有强氧化性,消毒原理与84消毒液、双氧水一样;光见不会分解的KOH不需要保存在棕色试剂瓶中;由转化关系图知KOH及MnO2会被循环利用。由3K2MnO4+CO2=2KMnO4+K2CO3+MnO2知,1mol K2MnO4在反应中能得到![]() mol KMnO4,而最初的原料中1mol MnO2恰好得到1mol KMnO4。
mol KMnO4,而最初的原料中1mol MnO2恰好得到1mol KMnO4。
因盐酸具有挥发性而硫酸没有,故应该用硫酸与纯碱反应来制CO2(CaSO4微溶)。操作I是将固化与液体分开,属于过滤;操作II是将两种可溶于性盐分离开,应该是利用物质溶解度的差异,通过浓缩结晶的方式将二者分离开。