题目内容
工业上利用下列反应消除氮氧化物的污染:
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol
在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得甲烷的物质的量随时间变化数据如下表:
下列说法不正确的是( )
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol
在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得甲烷的物质的量随时间变化数据如下表:
| 温度 | 时间/min/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | b | … | 0.15 |
| A、T1时0-10min时间段反应速率v(NO2)=0.30mol?L-1?min-1 |
| B、温度:T1<T2 |
| C、b>0.20 |
| D、△H:a<0 |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:A、根据v=
计算出CH4的速率,根据速率之比等于计量数之比,由化学方程式可知,二氧化氮与甲烷的计量数之比为2:1,可求得二氧化氮的速率,据此作判断;
B、由题中数据可知,在前10min时,在温度T1下CH4减小了0.5mol-0.35mol=0.15mol,在T2时,CH4减小了0.5mol-0.30mol=0.20mol,所以在T2时反应速率快,所以温度:T1<T2,据此作判断;
C、温度高反应速率快,所以在10min到20min之间,T2大于T1,所以甲烷的变化量T2时大于T1时的,而T1时变化了0.1mol,所以在20min时,T2条件下b<0.20,据此作判断;
D、由于T2大于T1,而在T2平衡时甲烷的物质的量为0.15大于T1时的0.1,平衡逆向移动,所以该反应为放热反应,即a<0,据此作判断.
| △c |
| t |
B、由题中数据可知,在前10min时,在温度T1下CH4减小了0.5mol-0.35mol=0.15mol,在T2时,CH4减小了0.5mol-0.30mol=0.20mol,所以在T2时反应速率快,所以温度:T1<T2,据此作判断;
C、温度高反应速率快,所以在10min到20min之间,T2大于T1,所以甲烷的变化量T2时大于T1时的,而T1时变化了0.1mol,所以在20min时,T2条件下b<0.20,据此作判断;
D、由于T2大于T1,而在T2平衡时甲烷的物质的量为0.15大于T1时的0.1,平衡逆向移动,所以该反应为放热反应,即a<0,据此作判断.
解答:
解:A、根据v=
计算出CH4的速率为
mol?L-1?min-1=0.015mol?L-1?min-1,根据速率之比等于计量数之比,由化学方程式可知,二氧化氮与甲烷的计量数之比为2:1,可求得二氧化氮的速率为0.030mol?L-1?min-1,故A错误;
B、由题中数据可知,在前10min时,在温度T1下CH4减小了0.5mol-0.35mol=0.15mol,在T2时,CH4减小了0.5mol-0.30mol=0.20mol,所以在T2时反应速率快,所以温度:T1<T2,故B正确;
C、温度高反应速率快,所以在10min到20min之间,T2大于T1,所以甲烷的变化量T2时大于T1时的,而T1时变化了0.1mol,所以在20min时,T2条件下b<0.20,故C错误;
D、由于T2大于T1,而在T2平衡时甲烷的物质的量为0.15大于T1时的0.1,平衡逆向移动,所以该反应为放热反应,即a<0,故D正确;
故选AC.
| △c |
| t |
| ||
| 10 |
B、由题中数据可知,在前10min时,在温度T1下CH4减小了0.5mol-0.35mol=0.15mol,在T2时,CH4减小了0.5mol-0.30mol=0.20mol,所以在T2时反应速率快,所以温度:T1<T2,故B正确;
C、温度高反应速率快,所以在10min到20min之间,T2大于T1,所以甲烷的变化量T2时大于T1时的,而T1时变化了0.1mol,所以在20min时,T2条件下b<0.20,故C错误;
D、由于T2大于T1,而在T2平衡时甲烷的物质的量为0.15大于T1时的0.1,平衡逆向移动,所以该反应为放热反应,即a<0,故D正确;
故选AC.
点评:本题主要考查了化学反应速率的计算、影响化学反应速率的因素及影响平衡移动的因素等知识点,难度不大,解题时要注意基础知识的灵活运用.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
某互为同分异构体的两种有机物甲、乙的结构简式分别为: 和
和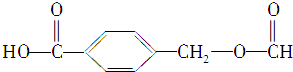 若各1mol该有机物在一定条件下与NaOH溶液反应,消耗NaOH的物质的量分别是( )
若各1mol该有机物在一定条件下与NaOH溶液反应,消耗NaOH的物质的量分别是( )
 和
和 若各1mol该有机物在一定条件下与NaOH溶液反应,消耗NaOH的物质的量分别是( )
若各1mol该有机物在一定条件下与NaOH溶液反应,消耗NaOH的物质的量分别是( )| A、3 mol、2 mol |
| B、2 mol、2 mol |
| C、3 mol、3 mol |
| D、5 mol、3 mol |
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H202相似,熔点为l93K,沸点为41lK,遇水很容易水解,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得.下列有关说法正确的是( )
| A、S2C12晶体中不存在离子键 |
| B、S2C12分子中各原子均达到8电子稳定结构 |
| C、S2C12在熔融状态下能导电 |
| D、S2C12与水反应后生成的气体难溶于水 |
现有常温下的四份溶液:①0.01mol/L HCl; ②0.01mol/L CH3COOH; ③pH=12的氨水;④pH=12的NaOH溶液.下列说法正确的是( )
| A、②中由水电离出的c(H+)=1×10-12mol/L |
| B、将①、③混合,若有pH=7,则消耗溶液的体积:③>① |
| C、将②、④等体积混合(体积变化忽略不计),则c(CH3COO-)+c(CH3COOH)=0.01 mol/L |
| D、将四份溶液均稀释10倍以后的溶液pH:③>④,②>① |
下列有关化学用语正确的是( )
| A、次氯酸的结构式:H-Cl-O |
B、二氧化碳的比例模型: |
C、甲基的电子式: |
| D、纤维素的通式:(C6H12O6)n |
下列命名错误的是( )
| A、4-乙基-3-戊醇 |
| B、2-甲基-1-丁醇 |
| C、2-甲基-1-丙醇 |
| D、4-甲基-2-己醇 |
已知:2M(g)?N(g);△H<0.现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如图所示.下列说法正确的是( )
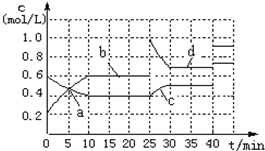

| A、a、b、c、d四个点中处于平衡状态的点是a、b |
| B、反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C、若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D、若40min后出现如图所示变化,则可能是加入了某种催化剂 |
下列实验操作中,正确的是( )
| A、蒸发溶液时,边加热加搅拌,直至蒸发皿内的液体蒸干 |
| B、量取25.00LKMnO4溶液时,应选择酸式滴定管 |
| C、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4注入容量瓶中加水稀释,边注入边搅拌 |
| D、配制一定物质的量浓度的溶液时,若未洗涤烧杯和玻璃棒,则会导致所配溶液的物质的量浓度偏高 |