题目内容
11.常温常压下,将NH3缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入CO2,整个实验过程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发).下列叙述正确的是( )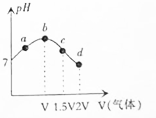
| A. | d点所示溶液中:c(NH4+)+c(NH3•H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| B. | a点到b点的过程中,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| C. | c点所示溶液中,c(CO32-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性 |
分析 A.d点是氯化铵溶液和碳酸氢钠饱和溶液,溶液中存在氮物料守恒,碳元素守恒,析出碳酸氢钠,则溶液中氯离子大于溶液中钠离子;
B.a点到b点是向饱和氯化钠溶液中通入氨气达到饱和,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$×$\frac{c(O{H}^{-})}{c(O{H}^{-})}$=$\frac{1}{{K}_{b}.c(O{H}^{-})}$;
C.c点所示溶液是碳酸铵溶液,图象分析可知溶液显碱性;
D.b到c点是一水合氨和通入的二氧化碳反应得到碳酸铵溶液,c到d点是碳酸铵和二氧化碳反应生成碳酸氢铵,在溶液中依据溶解度大小最后反应生成碳酸氢钠晶体和氯化铵溶液.
解答 解:A.d点是氯化铵溶液和碳酸氢钠饱和溶液,溶液中存在氮物料守恒,碳元素守恒,析出碳酸氢钠,则溶液中氯离子大于溶液中钠离子,c(NH4+)+c(NH3•H2O)>c(HCO3-)+c(CO32-)+c(H2CO3),故A错误;
B.a点到b点是向饱和氯化钠溶液中通入氨气达到饱和,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$×$\frac{c(O{H}^{-})}{c(O{H}^{-})}$=$\frac{1}{{K}_{b}.c(O{H}^{-})}$,生成一水合氨的过程中,溶液中氢氧根离子浓度增大,则溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$减小,故B错误;
C.c点所示溶液是碳酸铵溶液,图象分析可知溶液显碱性,离子浓度大小为:c(NH4+)>c(CO32-)>c(OH-)>c(H+),故C错误;
D.b到c点是一水合氨和通入的二氧化碳反应得到碳酸铵溶液,c到d点是碳酸铵和二氧化碳反应生成碳酸氢铵,在溶液中依据溶解度大小最后反应生成碳酸氢钠晶体和氯化铵溶液,由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性,故D正确;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生识图能力及分析判断能力,明确曲线变化趋势及每一点物质成分是解本题关键,题目难度中等.

 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案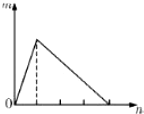 将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情况的一组物质是( )
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情况的一组物质是( )| A | B | C | D | |
| X | Ba(OH)2 | NaOH | NH3 | HCl |
| Y | 明矾 | AlCl3 | MgSO4 | NaAlO2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | Al溶于NaOH溶液:2Al+2H2O+2NaOH═2NaAlO2+3H2↑ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| C. | 向FeCl3溶液中滴加淀粉碘化钾溶液,溶液变蓝:2Fe3++2I-═2Fe2++I2 | |
| D. | 红热的Fe丝与水接触,表面形成蓝黑色保护层:2Fe+3H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$ Fe2O3+3H2↑ |
| A. | 乙醛和甲酸两者都能发生银镜反应,所以它们互为同系物 | |
| B. | 营养物质中的多糖、油脂、蛋白质在一定条件下都可以发生水解 | |
| C. | 氨基酸和氯乙烯都能通过加聚反应生成高分子化合物 | |
| D. | 通过对煤的分馏,可以提高煤的利用率 |
| A. | Ba2+ | B. | Na+ | C. | OH- | D. | Ag+ |
| A. | 通常用来衡量一个国家的石油化学工业发展水平的标志是石油产量 | |
| B. | 只要存在离子键的化合物就是离子化合物 | |
| C. | NH3的电子式为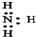 | |
| D. | 原电池中活泼的金属做正极 |
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向盛有2mL0.1mol/L AgNO3溶液的试管中,先滴加几滴0.1mol/L KCl溶液,再滴加0.1mol/L KI溶液 | 先出现白色沉淀,后出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 将适量CO2和SO2分别通入装有Ba(NO3)2溶液的两支试管中 | 一支试管出现白色沉淀,另一支试管无明显现象 | 出现的白色沉淀是BaSO3 |
| C | 取少量KClO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液 | 产生白色沉淀 | KClO3中含Cl- |
| D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y可能是Cl2 |
| A. | A | B. | B | C. | C | D. | D |