题目内容
将12.4 g NaOH和NaHCO3组成的固体混合物置于密闭容器中,加热到250 ℃,经充分反应后排出气体,冷却后称量剩余固体质量为10.6 g。试求原混合物中NaOH的质量分数。
32%
解析:
根据题干提示信息,已知NaOH与NaHCO3的总质量,所以两者之间的反应有以下三种情况:
(1)恰好完全反应,
NaOH+NaHCO3══Na2CO3+H2O
固体减少的质量等于生成的水的质量
(2)NaHCO3过量,则发生以下两个反应
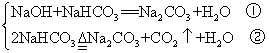
固体减少的质量等于第一个反应生成的水的质量与第二个反应生成的H2O、CO2质量之和。
(3)NaOH过量
NaOH+NaHCO3══Na2CO3+H2O
固体减少的质量等于生成的水的质量,但H2O的质量比第一种情况要小,首先分析第一种情况
①2NaHCO3![]() Na2CO3+H2O↑+CO2↑
Na2CO3+H2O↑+CO2↑
生成的CO2被NaOH吸收:
②2NaOH+CO2![]() Na2CO3+H2O↑
Na2CO3+H2O↑
因此NaOH与CO2的反应有三种情况:
(1)NaOH不足,CO2有剩余;
(2)CO2不足,NaOH有剩余;
(3)NaOH和CO2恰好完全反应,二者都无剩余。先分析第(3)种情况。此时,混合物中NaHCO3与NaOH的物质的量之比为1∶1,相当于发生下列反应:
③![]()
![]() Na2CO3+H2O↑
Na2CO3+H2O↑
124 g 18 g
12.4 g m(H2O)
m(H2O)=![]() =1.8 g。
=1.8 g。
由于题干中12.4 g固体混合物完全反应后,也是失重1.8 g
所以原固体混合物中:
n(NaOH)∶n(NaHCO3)=1∶1。
则原混合物中NaOH的质量分数为:
w(NaOH)=![]() =
=![]() ×100%=32%。
×100%=32%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.0.5 L 1 mol/L NaHS溶液中,N(Na+)+N(HS—)=NA |
| B.12.4 g白磷(分子式为P4)中含有P—P共价键0.6 NA |
| C.常温下,pH=2的醋酸溶液中所含有的H+数为0.01 NA |
| D.将92 g N2O4晶体放入容器中,恢复到常温常压时,所含气体分子数为NA |