题目内容
8.下列说法正确的是( )| A. | 苯酚不慎沾到皮肤上,要先用氢氧化钠溶液清洗,再用水洗 | |
| B. | 被蜜蜂或者蚂蚁蛰了以后痛痒难忍,可以用稀硼酸溶液清洗被蛰处,可减轻痛痒 | |
| C. | 浓硝酸不慎滴到皮肤上,皮肤变成黄色,是因为发生了颜色反应 | |
| D. | 甘油和乙二醇都可以用做抗冻剂,是因为这两个物质的凝固点比较低 |
分析 A.氢氧化钠具有腐蚀性;
B.蚊虫叮咬后,会释放出蚁酸,应用碱性物质中和;
C.浓硝酸与蛋白质发生颜色反应;
D.甘油和乙二醇都可以用做抗冻剂,是由于甘油和乙二醇的水溶液的凝固点比较低.
解答 解:A.苯酚易溶于酒精,苯酚不慎沾到皮肤上,可用酒精擦洗,因氢氧化钠具有腐蚀性,不能用氢氧化钠,故A错误;
B.蚊虫叮咬后,会释放出蚁酸,应用碱性物质中和,可用肥皂水,故B错误;
C.浓硝酸与蛋白质发生颜色反应,变黄色,故C正确;
D.甘油和乙二醇都可以用做抗冻剂,是由于甘油和乙二醇的水溶液的凝固点比较低,故D错误.
故选C.
点评 本题综合考查有机物的性质与应用,为高频考点,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累,难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
19.下列说法中正确的是( )
| A. | SO2、CO2、SiO2中的S、C、Si均为sp3杂化 | |
| B. | SO32-、CO32-、SiO32-均为平面三角形 | |
| C. | H3O+、NH4+、[Cu(NH3)4]2+均含有配位键 | |
| D. | 石墨、新型高分子导电材料聚乙炔、金属晶体均含有金属键 |
16.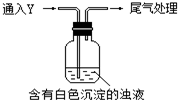 某校探究性活动小组的同学对Na2SO3与AgNO3在不同的pH条件下的反应原理进行实验探究,请你一起参与探究活动并回答有关问题:
某校探究性活动小组的同学对Na2SO3与AgNO3在不同的pH条件下的反应原理进行实验探究,请你一起参与探究活动并回答有关问题:
(1)测得Na2SO3溶液pH=10,AgNO3溶液pH=5,二者水解的离子分别是SO32-、Ag+.
(2)调节pH,实验记录如表:
查阅资料得知:
ⅰ.Ag2SO3:白色,难溶于水,溶于过量的Na2SO3溶液
ⅱ.Ag2O:棕黑色,不溶于水,能和酸反应
①推测a中白色沉淀为Ag2SO3,离子方程式是2Ag++SO32-=Ag2SO3↓.
②推测a中白色沉淀为Ag2SO4,推测的依据是SO32-有还原性,可能被氧化为SO42-,与Ag+反应生成Ag2SO4白色沉淀.
(3)取b、c中白色沉淀,置于Ag2SO3溶液中,沉淀溶解.该同学设计实验确认了白色沉淀不是Ag2SO4,实验方法是:另取Ag2SO4固体置于过量Na2SO3溶液中,未溶解.
(4)将c中X滤出、洗净,为确认其组成,实验如下:
Ⅰ.向X中滴加稀盐酸,无明显变化
Ⅱ.向X中加入过量浓NHO3,产生红棕色气体
Ⅲ.用Ba(HO3)2、BaCl2检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀
①实验Ⅰ的目的是检验X是否为Ag2O.
②根据上述现象,分析X具有还原性;X中含有Ag元素,不含S元素.
③Ⅱ中反应的化学方程式是Ag+2HNO3(浓)═AgNO3+NO2↑+H2O.
(5)该同学综合以上实验,分析X产生的原因,认为随着酸性的增强,体系还原性增强.通过进一步实验确认了这种可能性,实验如下:
①气体Y是SO2.
②白色沉淀转化为X的化学方程式是:Ag2SO3+H2O=2Ag+H2SO4.
 某校探究性活动小组的同学对Na2SO3与AgNO3在不同的pH条件下的反应原理进行实验探究,请你一起参与探究活动并回答有关问题:
某校探究性活动小组的同学对Na2SO3与AgNO3在不同的pH条件下的反应原理进行实验探究,请你一起参与探究活动并回答有关问题:(1)测得Na2SO3溶液pH=10,AgNO3溶液pH=5,二者水解的离子分别是SO32-、Ag+.
(2)调节pH,实验记录如表:
| 实验 | pH | 实 验 现 象 |
| a | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
| b | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
| c | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
ⅰ.Ag2SO3:白色,难溶于水,溶于过量的Na2SO3溶液
ⅱ.Ag2O:棕黑色,不溶于水,能和酸反应
①推测a中白色沉淀为Ag2SO3,离子方程式是2Ag++SO32-=Ag2SO3↓.
②推测a中白色沉淀为Ag2SO4,推测的依据是SO32-有还原性,可能被氧化为SO42-,与Ag+反应生成Ag2SO4白色沉淀.
(3)取b、c中白色沉淀,置于Ag2SO3溶液中,沉淀溶解.该同学设计实验确认了白色沉淀不是Ag2SO4,实验方法是:另取Ag2SO4固体置于过量Na2SO3溶液中,未溶解.
(4)将c中X滤出、洗净,为确认其组成,实验如下:
Ⅰ.向X中滴加稀盐酸,无明显变化
Ⅱ.向X中加入过量浓NHO3,产生红棕色气体
Ⅲ.用Ba(HO3)2、BaCl2检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀
①实验Ⅰ的目的是检验X是否为Ag2O.
②根据上述现象,分析X具有还原性;X中含有Ag元素,不含S元素.
③Ⅱ中反应的化学方程式是Ag+2HNO3(浓)═AgNO3+NO2↑+H2O.
(5)该同学综合以上实验,分析X产生的原因,认为随着酸性的增强,体系还原性增强.通过进一步实验确认了这种可能性,实验如下:
①气体Y是SO2.
②白色沉淀转化为X的化学方程式是:Ag2SO3+H2O=2Ag+H2SO4.
3.已知25℃时下列酸的电离平衡常数:K(CH3COOH)=1.75×10-5、K(HCN)=6.2×10-10、K1(H2CO3)=4.2×10-7、K2(H2CO3)=5.6×10-11下列选项不正确的是( )
| A. | 过量CO2通入溶液中:2NaCN+H2O+CO2=2HCN+Na2CO3 | |
| B. | 经测定CH3COONH4的水溶液呈中性可知:K(NH3•H2O)=1.75×10-5 | |
| C. | 将等物质的量浓度的CH3COONa与NaCN溶液等体积混合后的溶液中:c(CH3COO-)>c(CN-) | |
| D. | 常温下将10ml的PH=3的醋酸溶液稀释到100ml,其PH<4 |
20.反应2SO2(g)+O2(g)═2SO3(g)经一段时间后,SO3的浓度增加了0.4mol•L-1,在这段时间内用O2表示的反应速率为0.04mol•L-1•s-1,则这段时间为C( )
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
17.下列气体中,无色而有刺激性气味的是( )
| A. | N2 | B. | NO | C. | SO2 | D. | NO2 |
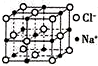 由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.
由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症. ,未成对电子数为5.
,未成对电子数为5.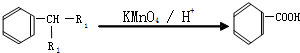
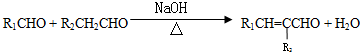 (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基)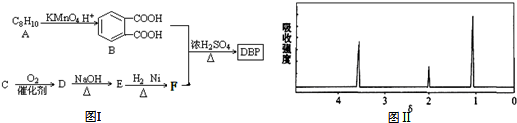
 ,该反应的反应类型为取代反应或酯化反应.
,该反应的反应类型为取代反应或酯化反应.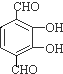 、
、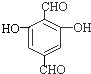 等.
等.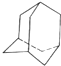 油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: