题目内容
U、W、X、Y、Z都是短周期元素,且原子序数依次增大.其中U与W可形成三角锥形分子甲,U与X可形成常温下呈液态的分子乙,甲、乙均为10 电子分子;Y 元素原子的 K 层电子数与M层电子数相同;Z元素的单质、氧化物均为原子晶体.请回答下列问题:
(1)Z元素在周期表中的位置 .
(2)X、Y、Z三种元素的原子半径由小到大的顺序是 (用元素符号表示).
(3)U与X形成的18电子化合物的电子式是 .
(4)ZX2与NaOH溶液反应的化学方程式是 .
(5)已知:N2(g)+3H2 (g)═2NH3 (g)△H═-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H═-483.6kJ/mol
试写出氨气完全燃烧生成气态水的热化学方程式 .
(1)Z元素在周期表中的位置
(2)X、Y、Z三种元素的原子半径由小到大的顺序是
(3)U与X形成的18电子化合物的电子式是
(4)ZX2与NaOH溶液反应的化学方程式是
(5)已知:N2(g)+3H2 (g)═2NH3 (g)△H═-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H═-483.6kJ/mol
试写出氨气完全燃烧生成气态水的热化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:U、W、X、Y、Z都是短周期元素,且原子序数依次增大.其中U与W可形成三角锥形分子甲,则U为H,W为N,甲为NH3,U与X可形成常温下呈液态的分子乙,甲、乙均为10电子分子,则X为O,乙为H2O;Y元素原子的K层电子数与M层电子数相同,则Y为Mg;Z元素的单质、氧化物均为原子晶体,则Z为Si,据此答题.
解答:
解:U、W、X、Y、Z都是短周期元素,且原子序数依次增大.其中U与W可形成三角锥形分子甲,则U为H,W为N,甲为NH3,U与X可形成常温下呈液态的分子乙,甲、乙均为10电子分子,则X为O,乙为H2O;Y元素原子的K层电子数与M层电子数相同,则Y为Mg;Z元素的单质、氧化物均为原子晶体,则Z为Si,
(1)Si的质子数为14,位于第三周期ⅣA族,
故答案为:第三周期ⅣA族;
(2)原子的电子层数越多,半径越大,同周期元素从左向右原子半径在减小,则原子半径为O<N<Si<Mg,
故答案为:O<N<Si<Mg;
(3)U与X形成的18电子化合物为H2O2,其电子式为 ,
,
故答案为: ;
;
(4)SiO2与NaOH溶液反应的化学方程式为SiO2+2NaOH=Na2SiO3+H2O,
故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(5)已知:①N2(g)+3H2 (g)═2NH3 (g)△H═-92.4kJ/mol;②2H2(g)+O2(g)═2H2O(g)△H═-483.6kJ/mol,根据盖斯定律,将②×3-①×2可得氨气完全燃烧生成气态水的热化学方程式为4NH3 (g)+3O2(g)═2N2(g)+6H2O(g)△H═-1266kJ/mol,
故答案为:4NH3 (g)+3O2(g)═2N2(g)+6H2O(g)△H═-1266kJ/mol.
(1)Si的质子数为14,位于第三周期ⅣA族,
故答案为:第三周期ⅣA族;
(2)原子的电子层数越多,半径越大,同周期元素从左向右原子半径在减小,则原子半径为O<N<Si<Mg,
故答案为:O<N<Si<Mg;
(3)U与X形成的18电子化合物为H2O2,其电子式为
 ,
,故答案为:
 ;
;(4)SiO2与NaOH溶液反应的化学方程式为SiO2+2NaOH=Na2SiO3+H2O,
故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(5)已知:①N2(g)+3H2 (g)═2NH3 (g)△H═-92.4kJ/mol;②2H2(g)+O2(g)═2H2O(g)△H═-483.6kJ/mol,根据盖斯定律,将②×3-①×2可得氨气完全燃烧生成气态水的热化学方程式为4NH3 (g)+3O2(g)═2N2(g)+6H2O(g)△H═-1266kJ/mol,
故答案为:4NH3 (g)+3O2(g)═2N2(g)+6H2O(g)△H═-1266kJ/mol.
点评:本题主要考查了元素周期律、电子式、化学反应方程式及盖斯定律等知识,难度不大,解题的关键是元素推断.

练习册系列答案
相关题目
在2H2S+SO2═2H2O+3S中氧化产物与还原产物质量之比为( )
| A、2:1 | B、1:2 |
| C、3:2 | D、2:3 |
常温下,在溶液中可发生以下反应:由此判断下列说法错误的是( )
①16H++10Z-+2XO4-═2X2++5Z2+8H2O;
②2M2++R2═2M3++2R-;
③2R-+Z2═R2+2Z-.
①16H++10Z-+2XO4-═2X2++5Z2+8H2O;
②2M2++R2═2M3++2R-;
③2R-+Z2═R2+2Z-.
| A、常温下可发生反应2M2++Z2═2M3++2Z- |
| B、还原性强弱顺序为:X2+<Z-<R-<M2+ |
| C、Z元素在反应①中被氧化,在③中被还原 |
| D、氧化性强弱顺序为:XO4-<Z2<R2<M3+ |
 短周期元素R、Q、M、T在元素周期表中的相对位置如图1,已知R原子最外层电子数与次外层电子数之比为2:1.
短周期元素R、Q、M、T在元素周期表中的相对位置如图1,已知R原子最外层电子数与次外层电子数之比为2:1.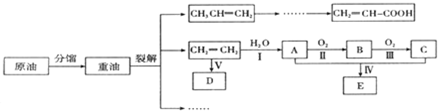
 Ⅰ.25℃时,在20ml Ba(OH)2溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,试回答以下问题:
Ⅰ.25℃时,在20ml Ba(OH)2溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,试回答以下问题: