题目内容
19.下列装置所示的实验能达到目的是( )| A. |  检验装置气密性 | B. | 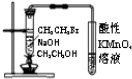 验证溴乙烷发生消去反应生成乙烯 | ||
| C. |  测定中和热 | D. | 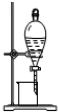 从碘的CCl4溶液中分离出碘 |
分析 A.关闭指示剂,利用液柱法检验气密性;
B.乙醇易挥发,乙醇、乙烯均能被高锰酸钾氧化;
C.图中缺少环形玻璃搅拌棒;
D.碘的CCl4溶液不分层.
解答 解:A.关闭指示剂,加液体后,导管内液面与烧瓶中液面存在一段液柱,其高度一段时间不变,则气密性良好,故A正确;
B.乙醇易挥发,乙醇、乙烯均能被高锰酸钾氧化,则不能检验乙烯,故B错误;
C.图中缺少环形玻璃搅拌棒,不能准确测定最高温度,故C错误;
D.碘的CCl4溶液不分层,不能利用图中分液漏斗分离,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及气密性检验、物质检验、中和热测定及混合物分离提纯,把握物质的性质、实验装置的作用、实验技能为解答关键为解答该题的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列有关0.1L 0.1mol/LKMnO4酸性溶液的叙述正确的是( )
| A. | 与少量乙二醛混合可制备乙二酸 | |
| B. | 与浓盐酸反应的离子方程式为:2MnO4-+16 H++10Cl-=5Cl2↑+2Mn2++8 H20 | |
| C. | 与K+、NO3-、SO42-、CO32-可以大量共存 | |
| D. | 与过量Na202混合后,共转移e-0.05mol |
4.下列分子在限定条件下的同分异构体数目不为4的是( )
| A. | C4H8O2属于酯的同分异构体 | B. | C5H10O2属于酸的同分异构体 | ||
| C. | 甲苯的一氯取代物 | D. | 化合物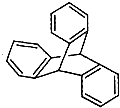 的一氯取代物 的一氯取代物 |
11. 对PM2.5、SO2、NOx等进行研究,有助于了解雾霾和减弱雾霾的影响.请回答下列问题:
对PM2.5、SO2、NOx等进行研究,有助于了解雾霾和减弱雾霾的影响.请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据计算PM2.5试样的pH为4.
(2)为了减少污染,可对含SO2的烟气进行洗涤,以下物质可作洗涤剂的是B.
A.BaCl2 B.Ca(OH)2 C.HNO3 D.NaHSO3
(3)NOx是汽车尾气中的主要污染物之一,在汽车尾气系统中安装催化转化器,可有效降低NOX的排放.
①当尾气中空气不足时,NOX在催化转化器中被还原成N2排出,已知信息如下:
N2(g)+O2(g)═2NO(g)△H1=+180kJ/mol
2C(s)+O2(g)═2CO(g)△H2=-222kJ/mol
C(s)+O2(g)═CO2(g)△H3=-394kJ/mol
则NO(g)与CO(g)进行催化转化的热化学方程式为2NO(g)+2CO(g)=N2(g)+CO2(g)△H═-746KJ/mol.
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOX生成硝酸盐,然后将硝酸盐溶于水,可用电化学降解来治理水中硝酸盐的污染,在酸性条件下,电解NO3-的原理如图所示:写出阴极电极反应式2NO3-+10e-+12H+=6H2O+N2↑.
 对PM2.5、SO2、NOx等进行研究,有助于了解雾霾和减弱雾霾的影响.请回答下列问题:
对PM2.5、SO2、NOx等进行研究,有助于了解雾霾和减弱雾霾的影响.请回答下列问题:(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度(mol•L-1) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为了减少污染,可对含SO2的烟气进行洗涤,以下物质可作洗涤剂的是B.
A.BaCl2 B.Ca(OH)2 C.HNO3 D.NaHSO3
(3)NOx是汽车尾气中的主要污染物之一,在汽车尾气系统中安装催化转化器,可有效降低NOX的排放.
①当尾气中空气不足时,NOX在催化转化器中被还原成N2排出,已知信息如下:
N2(g)+O2(g)═2NO(g)△H1=+180kJ/mol
2C(s)+O2(g)═2CO(g)△H2=-222kJ/mol
C(s)+O2(g)═CO2(g)△H3=-394kJ/mol
则NO(g)与CO(g)进行催化转化的热化学方程式为2NO(g)+2CO(g)=N2(g)+CO2(g)△H═-746KJ/mol.
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOX生成硝酸盐,然后将硝酸盐溶于水,可用电化学降解来治理水中硝酸盐的污染,在酸性条件下,电解NO3-的原理如图所示:写出阴极电极反应式2NO3-+10e-+12H+=6H2O+N2↑.
8.25℃时,下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1( NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 20 mL 0.1 mol•L-1 CH3COONa溶液与10 mL 0.1 mol•L-1 HCl溶液混合所得酸性溶液中:c(Na+)>c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合所得溶液中:c(CH3COO-)+c(H+)>c(Na+)+c(OH-) | |
| D. | 向浓度为0.1mol•L-1的NaHCO3溶液中滴加少量盐酸后所得溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
 和高分子化合物PCL的合成路线如下:
和高分子化合物PCL的合成路线如下:
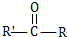 $\stackrel{过氧化物}{→}$
$\stackrel{过氧化物}{→}$ (R、R′代表烃基)
(R、R′代表烃基)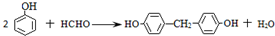 .
. .
.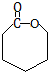 .高分子化合物PCL的结构简式是
.高分子化合物PCL的结构简式是 .
. 、
、 .
.