题目内容
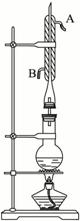
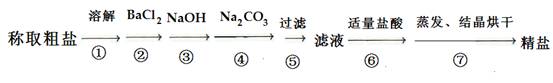
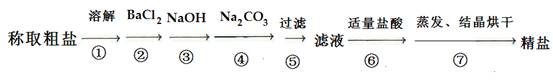
(14 分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)判断BaCl2 已过量的方法是____________________________
(2)第④步中,相关的离子方程式是____________________________
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是______________
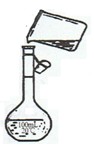
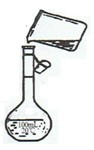
(4)为检验精盐纯度,需配制150mL0.2mol·L-1NaCl(精盐)溶液,如图是该同学 转移溶液的示意图,图中的错误是________________________________。
⑴取第②步后的上层清液1~2滴于滴定板上,再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(3分)
(2)Ca2++CO32-===CaCO3↓ (2 分)
Ba2+ +CO32- ===BaCO3↓(2分)
(3)在此酸度条件,会有部分沉淀溶解,从而影响制得精盐的纯度(3分)
(4)未用玻璃棒引流(2分);末采用l50mL容量瓶(2 分)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目