题目内容
3.下列依据相关实验得出的结论正确的是( )| A. | 向硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产生,说明Ksp(BaCO3)<Ksp(BaSO4) | |
| B. | 向淀粉溶液中加入稀硫酸并加热片刻,然后再加入适量银氨溶液进行水浴加热,没有银镜生成,说明淀粉没有水解 | |
| C. | 将二氧化硫气体通入到高锰酸钾酸性溶液中,溶液紫红色褪去,说明二氧化硫有漂白性 | |
| D. | 向碳酸钠溶液中滴加几滴酚酞试液,然后再加入氯化钡溶液,溶液红色褪去,说明碳酸钠溶液中存在水解平衡 |
分析 A.Ksp(BaCO3)>Ksp(BaSO4);
B.银镜反应应在碱性条件下进行;
C.二氧化硫与高锰酸钾发生氧化还原反应,高锰酸钾被还原而褪色;
D.Na2CO3溶液存在水解平衡,加氯化钡与碳酸根离子反应,水解平衡逆向移动.
解答 解:A.常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,部分BaSO4因饱和Na2CO3溶液中高浓度CO32-转化为BaCO3,因此向洗净的沉淀中加稀盐酸,有气泡产生,但是Ksp(BaCO3)>Ksp(BaSO4),故A错误;
B.淀粉在酸性条件下水解,而银镜反应应在碱性条件下进行,应先调节溶液呈碱性,故B错误;
C.将二氧化硫气体通入到酸性高锰酸钾溶液中,溶液褪色,体现了二氧化硫的还原性,故C错误;
D.Na2CO3溶液存在水解平衡,加氯化钡与碳酸根离子反应,水解平衡逆向移动,则红色逐渐褪去,故D正确.
故选D.
点评 本题考查化学实验方案的评价,涉及难溶电解质的溶解平衡、物质的检验、还原性以及盐类的水解等知识,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型和高频考点,注意把握实验的严密性和合理性,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 16 g O2中含有的氧分子数为NA | |
| B. | 1 mol Mg变为Mg2+时失去的电子数目为2NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1 mol•L-1 CaCl2溶液中含有的氯离子数为NA |
4.从香荚兰豆中提取的有机物A用来合成人工香料,其结构简式如图所示,下列关于物质A的说法正确的是( )
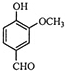

| A. | A的分子式是C8H10O3 | B. | A分子中含有酯基 | ||
| C. | A只能发生取代反应 | D. | A能与Na反应 |
11.下列实验操作中,正确的是( )
| A. | 配制5% NaCl溶液时,将已准确称量的NaCl放入烧杯中并加适量的水搅拌溶解 | |
| B. | 配制1mol•L-1 Na0H溶液时,将溶解后的NaOH溶液立即注入容量瓶 | |
| C. | 配制0.1mol•L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| D. | 配制1mol•L-1 Na2CO3溶液500mL,将Na2CO3放在托盘天平右盘称量 |
18.NaCl在生产中有重要作用.
(1)某小组用NaCl进行以下实验:
①Ⅰ中白色沉淀的化学式是AgCl.
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.
(1)某小组用NaCl进行以下实验:
| 步 骤 | 现 象 |
| Ⅰ.将NaCl溶液与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.将Ⅱ中经过滤洗得到的黑色沉淀分成两份,在一份沉淀中加蒸馏水,另一份沉淀中加入NaCl溶液,同时浸泡较长时间. | 加蒸馏水的沉淀仍为黑色,加入NaCl溶液的沉淀变为乳白色 |
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.
8.某化学兴趣小组用如图所示的药品和装置探究SO2气体的还原性:则下列说法不合理的是( )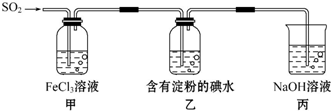

| A. | 为了验证Fe3+被SO2还原得到Fe2+,可向甲中加入KMnO4溶液,看紫红色是否褪去 | |
| B. | 甲中加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀说明SO2可以被Fe3+氧化 | |
| C. | 能表明I-的还原性弱于SO2的现象是乙中蓝色溶液褪色 | |
| D. | 装置丙的作用是吸收SO2尾气,防止污染空气 |
12.下列各组溶液,不另加其他试剂就可以将它们分别开的是( )
| A. | NaCl、HCl、NaAlO2、NaHCO3 | B. | NaSO4、KNO3、(NH4)2SO4、MgCl2 | ||
| C. | FeCl3、NaOH、AlCl3、HNO3 | D. | AgNO3、NaCl、NaSO4、NaI |
13.下列关于甲、乙、丙、丁四组仪器装置的有关用法正确且能达到目的是( )


| A. | 甲装置:可用来证明硫的非金属性比硅强 | |
| B. | 乙装置:用盐酸标准液测氢氧化钠溶液浓度 | |
| C. | 丙装置:配制一定物质的量浓度的氢氧化钠溶液 | |
| D. | 丁装置:可在瓶中先装满水,气体由②口入,收集NO气体 |