题目内容
在体积为100ml的密闭容器中,放入反应物A和B,在不同的温度下发生反应:2A(s)+B(g)?2C(g),得到该反应平衡常数与温度的关系如表所示.
下列说法正确的是( )
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A、加热平衡向右移动 |
| B、25℃时反应2C?2A(s)+B(g)的平衡常数为0.5 |
| C、在80℃时,测得某时刻,B、C浓度均为0.5mol/L,则此时v(正)>v(逆) |
| D、80℃达到平衡时,再投入一定量的A,平衡正向移动 |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:A、根据表格可知,温度越高平衡常数越小,说明平衡逆向移动,所以该反应的正反应为放热反应,加热平衡向左移动;
B、反应2C?2A(s)+B(g)为反应2A(s)+B(g)?2C(g)的逆反应,所以平衡常数也是互为倒数,所以25℃时反应2C?2A(s)+B(g)的平衡常数为
=2×10-5;
C、在80℃时,B、C浓度均为0.5mol/L,则此时浓度商Qc=
=0.5<2,所以平衡向正反应方向移动,即v(正)>v(逆);
D、A是固体物质,增加A的量,平衡不移动;
B、反应2C?2A(s)+B(g)为反应2A(s)+B(g)?2C(g)的逆反应,所以平衡常数也是互为倒数,所以25℃时反应2C?2A(s)+B(g)的平衡常数为
| 1 |
| 5×104 |
C、在80℃时,B、C浓度均为0.5mol/L,则此时浓度商Qc=
| 0.52 |
| 0.5 |
D、A是固体物质,增加A的量,平衡不移动;
解答:
解:A、根据表格可知,温度越高平衡常数越小,说明平衡逆向移动,所以该反应的正反应为放热反应,加热平衡向左移动,故A错误;
B、反应2C?2A(s)+B(g)为反应2A(s)+B(g)?2C(g)的逆反应,所以平衡常数也是互为倒数,所以25℃时反应2C?2A(s)+B(g)的平衡常数为
=2×10-5,故B错误;
C、在80℃时,B、C浓度均为0.5mol/L,则此时浓度商Qc=
=0.5<2,所以平衡向正反应方向移动,即v(正)>v(逆),故C正确;
D、A是固体物质,增加A的量,平衡不移动,故D错误;
故选C.
B、反应2C?2A(s)+B(g)为反应2A(s)+B(g)?2C(g)的逆反应,所以平衡常数也是互为倒数,所以25℃时反应2C?2A(s)+B(g)的平衡常数为
| 1 |
| 5×104 |
C、在80℃时,B、C浓度均为0.5mol/L,则此时浓度商Qc=
| 0.52 |
| 0.5 |
D、A是固体物质,增加A的量,平衡不移动,故D错误;
故选C.
点评:本题主要考查了影响平衡移动的外界因素、平衡常数的计算及应用,难度不大,本题A为固体,对平衡没有影响,是易错误点.

练习册系列答案
相关题目
下列有关摩尔质量的说法正确的是( )
| A、水的摩尔质量是18g |
| B、2mol水的摩尔质量是1mol水摩尔质量的2倍 |
| C、摩尔质量等于该粒子的相对原子质量或相对分子质量 |
| D、Na+的摩尔质量为23g/mol |
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
| A、Fe3+ K+ Cl- NO3- |
| B、Ag+ Na+ NO3- Cl- |
| C、Zn2+ Al3+ SO42- Cl- |
| D、Ba2+ NH4+ Cl- HCO3- |
 X、Y、Z、W四种短周期元素在周期表中的位置如图所示.已知这四种元素原子的核电荷数之和为36.则这四种元素按X、Y、Z、W顺序依次是( )
X、Y、Z、W四种短周期元素在周期表中的位置如图所示.已知这四种元素原子的核电荷数之和为36.则这四种元素按X、Y、Z、W顺序依次是( )| A、N、P、O、C |
| B、C、N、O、P |
| C、O、S、N、F |
| D、C、Si、Al、N |
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、足量Fe在1molCl2中充分燃烧,转移3NA个电子 |
| B、7.8gNa2O2中阴、阳离子总数为0.3NA |
| C、Cl2+H2O?HCl+HClO,若1molCl2参与反应,则转移NA个电子 |
| D、反应KClO3+6HCl═KCl+3Cl2+3H2O中,若有1molH2O生成,转移电子数为2NA |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A、一定有Cl- |
| B、一定有SO42- |
| C、一定没有Al3+ |
| D、一定有CO32- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴人酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- |
| B、能使红色石蕊试纸变蓝色的溶液中:K+、CO32-、NO3-、AlO2- |
| C、水电离产生的.(H+)=10-13mol/L的溶液中:Na+、Cl-、NO3-、CH3 COO- |
| D、pH=l 的溶液中:Na+、Fe2+、NO3-、Cl- |
将过量的SO2气体通入下列溶液中,最终没有沉淀的是( )
| A、Na[Al(OH)4] |
| B、BaCl2 |
| C、Ba(NO3)2 |
| D、Na2SiO3 |
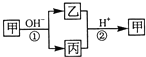 甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )| A、X元素可能为Al |
| B、X 元素不一定为非金属元素 |
| C、反应①和②互为可逆反应 |
| D、反应①和②一定为氧化还原反应 |