题目内容
下列溶液中的Cl-浓度与50mL 1mol/L AlCl3溶液中的Cl-浓度相等的是( )
| A、150mL 1mol/L NaCl |
| B、75mL 2mol/L NH4Cl |
| C、150mL 3mol/L KClO3 |
| D、75mL 1.5mol/L MgCl2 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L,根据溶质化学式计算各选项中的Cl-物质的量,进行比较可知.注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.
解答:
解:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L.
A、150ml1mol/L的NaCl溶液中Cl-浓度为1mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故A不符合;
B、75ml2mol/L的NH4Cl溶液中Cl-浓度为2mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故B不符合;
C、150ml3mol/L的KClO3溶液中无Cl-,故C不符合;
D、75ml 1.5mol/L的MgCl2溶液中Cl-浓度为3mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度相等,故D符合.
故选:D.
A、150ml1mol/L的NaCl溶液中Cl-浓度为1mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故A不符合;
B、75ml2mol/L的NH4Cl溶液中Cl-浓度为2mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故B不符合;
C、150ml3mol/L的KClO3溶液中无Cl-,故C不符合;
D、75ml 1.5mol/L的MgCl2溶液中Cl-浓度为3mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度相等,故D符合.
故选:D.
点评:本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
相关题目
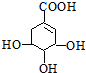 莽草酸是制取抗禽流感药物“达菲”的中间活性物质,其结构简式如图所示.从官能团的角度看莽草酸不属于( )
莽草酸是制取抗禽流感药物“达菲”的中间活性物质,其结构简式如图所示.从官能团的角度看莽草酸不属于( )| A、烯类 | B、酚类 | C、羧酸类 | D、醇类 |
向明矾[KAl(SO4)2?12H2O]溶液中滴入Ba(OH)2溶液时,当SO42-沉淀完全时,铝元素的存在形式是( )
| A、一部分为Al(OH)3沉淀,一部分以Al3+形式存在于溶液中 |
| B、一部分为Al(OH)3沉淀,一部分以[Al(OH)4]-形式存在于溶液中 |
| C、全部为Al(OH)3沉淀 |
| D、几乎全部以[Al(OH)4]-存在于溶液中 |
下列有关氧化还原反应的叙述中,正确的是( )
| A、一定有氧元素参加 |
| B、一定有电子转移(得失或偏移) |
| C、氧化反应一定先于还原反应发生 |
| D、氧化剂本身发生氧化反应 |
25℃,弱酸的电离平衡常数Ka如表所示,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
| A、pH相同的三种溶液物质的量浓度关系:c(Na2CO3)>c(NaCN)>c(CH3COONa) |
| B、a L 0.1mol?L-1CH3COOH与b L 0.1mol?L-1NaOH溶液混合后所得溶液中pH>7,则a一定小于或等于b |
| C、物质的量浓度和体积均相同的CH3COONa和NaOH两种溶液,已知前者溶液中离子数目为n1,后者溶液中离子数目为n2,则n1>n2 |
| D、物质的量浓度相同NaHCO3和Na2CO3的混合溶液中:2c(H+)-2c(OH-)=c(CO32-)-c(HCO3-)-c(H2CO3) |
只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称氢化物.下列物质属于氢化物的是( )
| A、H2CO3 |
| B、H2SO4 |
| C、NaH |
| D、HClO |