题目内容
香叶醇是合成玫瑰香油的主要原料,其结构简式如下,下列有关香叶醇的叙述不正确的是( )


| A、1mol香叶醇的完全燃烧需要消耗15mol O2 |
| B、能使溴的四氯化碳溶液褪色 |
| C、能使酸性高锰酸钾溶液褪色 |
| D、能发生加成反应和取代反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:该物质含2个C=C键、1个-OH,分子式为C10H18O,结合烯烃和醇的性质来解答.
解答:
解:A.分子式为C10H18O,1mol香叶醇的完全燃烧需要消耗(10+
-
)mol=14mol O2,故A错误;
B.含有碳碳双键,可与溴发生加成反应,故B正确;
C.碳碳双键和羟基可被酸性高锰酸钾氧化,故C正确;
D.含有碳碳双键,可发生加成反应,含有羟基,可发生取代反应,故D正确.
故选A.
| 18 |
| 4 |
| 1 |
| 2 |
B.含有碳碳双键,可与溴发生加成反应,故B正确;
C.碳碳双键和羟基可被酸性高锰酸钾氧化,故C正确;
D.含有碳碳双键,可发生加成反应,含有羟基,可发生取代反应,故D正确.
故选A.
点评:本题考查有机物的结构与性质,为高频考点,注意把握有机物的官能团与性质的关系,熟悉烯烃、醇的性质即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
25℃时,已知弱酸的电离常数:Ka(CH3COOH)=1.75×10-4,Ka1(H2CO3)=4.4×10-7,Ka2(HCO3-)=4.7×10-11,Ka(HClO)=4.0×10-8,则下列说法正确的是( )
| A、25℃时,0.1mol.L-1的酸性溶液比0.1mol.L-1的醋酸溶液的K值小 |
| B、25℃时,甲基橙滴入0.1mol.L-1醋酸溶液中,溶液呈黄色 |
| C、等物质的量浓度的碳酸钠溶液,醋酸钠溶液,醋氯酸钠溶液pH.pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |
| D、新制氯水中有次氯酸,水和氯气分子,所用新制氯水与碳酸氢钠不反应 |
用下列装置进行相应实验,能达到实验目的是( )
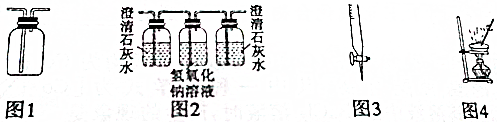

| A、用图1所示装置可以收集H2、NH3、CO2、NO2等气体 |
| B、用图2所示装置可以验证SO2气体中含有CO2气体 |
| C、用图3所示仪器可以量取Na2CO3溶液 |
| D、用图4所示装置可以进行硫酸铜晶体中结晶水含量的测定 |
下列各组离子一定能大量共存的是( )
| A、在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B、在能与Si反应产生H2的溶液中:NH4+、K+、SO32-、NO3- |
| C、在能与Al反应产生H2的溶液中:NH4+、Al3+、SO42-、NO3- |
| D、在pH=1的溶液中:K+、Fe3+、Cl-、NO3- |
下列醇不能发生消去反应的是( )
①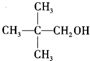 ②
② ③CH3OH ④
③CH3OH ④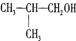
①
 ②
② ③CH3OH ④
③CH3OH ④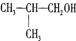
| A、①② | B、②④ | C、①③ | D、③④ |
将11.2g的Mg-Cu混合物完全溶解于足量的硝酸中收集反应产生的X气体,再向所得溶液中加入足量的NaOH溶液,产生21.4g沉淀.推断气体X的成分可能是( )
| A、0.3mo1NO2 |
| B、0.2mo1NO2和0.1mo1N2O4 |
| C、0.1mol NO、0.2mol NO2和0.05mol N2O4 |
| D、0.6mo1NO |