题目内容
5.X、Y、Z、W为周期表前四周期元素,其原子序数依次增大.X原子核外电子数等于其所在周期数,Y和Z基态原子最外层均有2个未成对电子,其中Y原子各能级电子数相同,Z原子核外电子占据5个原子轨道,W原子的价电子数是最外层电子数的5倍.(1)X、Y、Z三种元素按电负性从小到大的顺序为H<C<O.
(2)Y分别与X、Z形成两种最简单的非极性分子M和N,关于M和N的说法正确的是ac(填序号).
a.固态N属于分子晶体
b.M分子中含有极性共价键,所以易溶于水
c.M和N分子中心原子的杂化类型分别是sp3和sp
d.M中化学键键能小于N中化学键键能,所以M熔点低于N
(3)X与Z可形成两种常见化合物,其沸点均明显高于M和N,主要原因是水或双氧水分子间可以形成氢键,使其沸点升高
(4)在W催化作用下,M和N反应可获得化工原料YZ和X2.
①W的基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2,该元素在元素周期表中的位置第四周期第Ⅷ族.
②W能与化合物YZ形成正四面体形的配合物W(YZ)4,1mol W(YZ)4中含有8 molσ键.
(5)W单质晶体中原子堆积方式与Cu相同,其晶胞棱长为apm,请列出W单质晶体的密度表达式ρ=$\frac{4M}{{N}_{A}(a×1{0}^{-10})^{3}}$ g•cm-3( 用NA表示阿伏伽德罗常数的值,用M表示W的相对原子质量).
分析 X原子核外电子数等于其所在周期数,X为H元素;
Y和Z基态原子最外层均有2个未成对电子,其中Y原子各能级电子数相同,Z原子核外电子占据5个原子轨道,则Y为C元素,Z为O元素;
W原子的价电子数是最外层电子数的5倍,W为周期表前四周期元素,则W为28号元素Ni,
(1)非金属性越强电负性越大;
(2)正负电荷中心能重合的分子为非极性分子,Y分别与X、Z形成两种最简单的非极性分子M和N分别为CH4和CO2;
(3)氢键能增强分子间作用力;
(4)Ni属于28号元素,根据构造原理书写电子排布式;
(5)晶胞密度$ρ=\frac{m}{V}$.
解答 解:X原子核外电子数等于其所在周期数,X为H元素;
Y和Z基态原子最外层均有2个未成对电子,其中Y原子各能级电子数相同,Z原子核外电子占据5个原子轨道,则Y为C元素,Z为O元素;
W原子的价电子数是最外层电子数的5倍,W为周期表前四周期元素,则W为28号元素Ni,
(1)元素非金属性越强电负性越大,三种元素按电负性从小到大的顺序为H<C<O,故答案为:H<C<O;
(2)Y分别与X、Z形成两种最简单的非极性分子M和N分别为CH4和CO2,
a、固态CO2属于分子晶体,故a正确;
b.CH4分子中含有极性共价键,不溶于水,故b错误;
c.CH4和CO2分子中心原子的杂化类型分别是sp3和sp,故c正确;
d.CH4中化学键键能小于CO2中化学键键能,说明CO2比CH4稳定,和熔点无关,
故答案为:ac;
(3)H与O可形成两种常见化合物水和双氧水分子间含有氢键,分子间作用力增大,使沸点均明显高于CH4和CO2,
故答案为:水或双氧水分子间可以形成氢键,使其沸点升高;
(4)①Ni属于28号元素,基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2,属于第四周期第Ⅷ族元素,
故答案为:1s22s22p63s23p63d84s2或[Ar]3d84s2;第四周期第Ⅷ族;
②Ni能与化合物CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有8molσ键,
故答案为:8;
(5)Ni单质晶体中原子堆积方式与Cu相同,采用面心立方最密堆积,一个晶胞中含有Ni原子数为$8×\frac{1}{8}+6×\frac{1}{2}=4$,晶胞棱长为apm,所以Ni单质晶体的密度表达式ρ=$\frac{m}{V}$=$\frac{4M}{{N}_{A}(a×1{0}^{-10})^{3}}$.
故答案为:$\frac{4M}{{N}_{A}(a×1{0}^{-10})^{3}}$.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,综合考查学生分析能力、逻辑推理能力及对知识的迁移运用,需要学生具备扎实的基础,难度中等.

原反应的是( )
| A. | 铁杵成针 | B. | 抱薪救火 | C. | 闭门造车 | D. | 刻舟求剑 |
| A. | 由C(s,石墨)═C(s,金钢石)△H>0可知,金刚石比石墨稳定 | |
| B. | CO(g)燃烧热是283.0 kJ•mol-1,则2CO2(g)═2CO(g)+O2(g)△H=+566.0kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2+2H2O(I)△H<0,该反应的化学能可以转化为电能 | |
| D. | 已知C(s)+O2(g)═CO2(g)△H1,C(s)+$\frac{1}{2}$O2(g)═CO(g)△H2,则)△H1<△H2 |
| A. | 未加NaOH溶液时:c(H+)>c(Cl-)=c(CH3COOH) | |
| B. | 加入l0mLNaOH溶液时:c(CH3COO-)+c(OH-)=c(H+) | |
| C. | 加入20mLNaOH溶液时:c(Na+)=c(CH3COOH)+c(CH3COO一) | |
| D. | 加入20mLNaOH溶液时,酸碱恰好中和:c(OH-)=c(H+) |
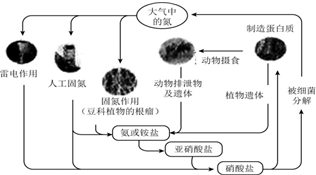
| A. | 上述氮循环中氮元素均被氧化 | |
| B. | 打雷闪电时涉及的一个反应为N2+2O2═2NO2 | |
| C. | 含氮无机物和含氮有机物可相互转化 | |
| D. | 自然界氮循环中氮元素的质量增加了 |
| A. | 0.1 mol•L-1的NaOH溶液中:K+、Na+、SO42-、CO32- | |
| B. | 0.1 mol•L-1的Na2CO3溶液中:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1 mol•L-1的FeCl3溶液中:K+NH4+、I-、SCN- | |
| D. | 0.1 mol•L-1的盐酸中:Fe2+、Na+、Br-、NO3- |
| A. | 液氨、液氯、干冰、碘化银均为化合物 | |
| B. | 明矾、小苏打、醋酸、次氯酸均为电解质 | |
| C. | 碘酒、牛奶、豆浆、漂白粉均为胶体 | |
| D. | Na2O2、Na2CO3、Na2SiO3、KNO3均为盐 |
| A. | Na2SO3溶液 | B. | NH4HCO3溶液 | C. | NaHCO3溶液 | D. | NaHSO3溶液 |
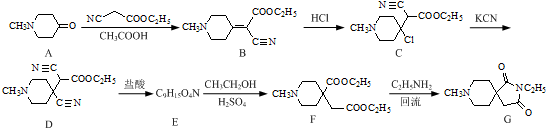
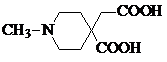 .
.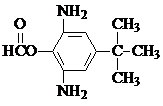 或
或 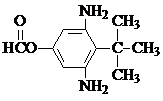 .
.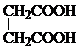 和CH3CH2Cl为原料制备
和CH3CH2Cl为原料制备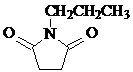 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: