题目内容
常温下在密闭容器中通入2mL某烷烃和13mLO2,点燃爆炸后去掉生成的CO2和H2O,再通入6mLO2,再点火爆炸,此时O2有剩余.通过计算求该烷烃的分子式和可能的结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:设烷烃的分子式为CnH2n+2,根据烷烃的燃烧通式CnH2n+2+(
)O2→nCO2+(n+1)H2O,根据题干信息可知,2mL该烃完全燃烧消耗氧气的体积大于13mL、小于(13+6)mL=19mL,据此列式讨论得出该烷烃的分子式,然后根据分子式确定该烷烃的同分异构体.
| 3n+1 |
| 2 |
解答:
解:设烃的分子式为CxHy,该烃的燃烧通式:CnH2n+2+(
)O2→nCO2+(n+1)H2O,
2mL某烷烃和13mLO2,点燃爆炸后去掉生成的CO2和H2O,再通入6mLO2,再点火爆炸,此时O2有剩余,说明2mL该烃完全燃烧消耗氧气的体积大于13mL、小于(13+6)mL=19mL,
即:
<
<
,
解得:4<n<6,
所以n=5,
该有机物为戊烷,分子式为:C5H12,
戊烷的同分异构体有:正戊烷 CH3CH2CH2CH2CH3、异戊烷 CH3CH(CH3)CH2CH3、新戊烷 C(CH3)4,
答:该烷烃的分子式为C5H12,C5H12的结构简式有三种:CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH3)4.
| 3n+1 |
| 2 |
2mL某烷烃和13mLO2,点燃爆炸后去掉生成的CO2和H2O,再通入6mLO2,再点火爆炸,此时O2有剩余,说明2mL该烃完全燃烧消耗氧气的体积大于13mL、小于(13+6)mL=19mL,
即:
| 13mL |
| 2mL |
| 3n+1 |
| 2 |
| 19mL |
| 2mL |
解得:4<n<6,
所以n=5,
该有机物为戊烷,分子式为:C5H12,
戊烷的同分异构体有:正戊烷 CH3CH2CH2CH2CH3、异戊烷 CH3CH(CH3)CH2CH3、新戊烷 C(CH3)4,
答:该烷烃的分子式为C5H12,C5H12的结构简式有三种:CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH3)4.
点评:本题考查了有机物分子式的确定、同分异构体的书写,题目难度中等,注意掌握常见有机物分子式、结构简式的确定方法,明确烷烃的燃烧通式为解答本题的关键.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
下列除去杂质的方法正确的是( )
| A、除去FeCl2溶液中的少量FeCl3:加入足量铁屑、充分反应后过滤 |
| B、除去CO2中的少量HCl:通入Na2CO3溶液、收集气体 |
| C、除去N2中的少量O2:通过灼热的CuO粉末、收集气体 |
| D、除去KCl溶液中的少量MgCl2:加入适量NaOH溶液、过滤 |
配制500mL 0.2mol?L-1 Na2SO4溶液,需要硫酸钠的质量是( )
| A、9.8g | B、14.2g |
| C、16g | D、32.2g |
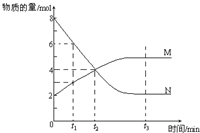 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2 N?M |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
有镁铝混合粉末10.2克,将它溶于500mL 4mol/L的盐酸中,若要使沉淀量最大,则需加入2mol/L的NaOH的体积为( )
| A、1000mL |
| B、500mL |
| C、100mL |
| D、1500mL |
有甲、乙、丙、丁四个集气瓶中分别盛有H2、Cl2、HCl、HBr中任意一种气体.若将甲和丙两气体混合,见光爆炸.若将丙、丁两气体混合后,瓶壁上出现深红棕色的液滴.则乙气体是( )
| A、H2 |
| B、Cl2 |
| C、HCl |
| D、HBr |
下列可以用来区分甲烷、乙烯、乙炔的是( )
| A、用溴水区分 |
| B、用酸性高锰酸钾溶液区分 |
| C、根据燃烧现象不同区分 |
| D、根据气味不同区分 |