题目内容
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂.其制备工艺流程如下:

已知:反应Ⅱ包含2NaHSO3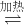 Na2S2O5+H2O等多步反应.
Na2S2O5+H2O等多步反应.
(1)反应I的化学方程式为______,反应Ⅰ进行时应先通入______气体.
(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,目的是______.在上述工艺流程中可循环使用的物质是______.
(3)反应Ⅱ中需控制参加反应的气体与固体的物质的量之比接近______,若气体量不足,则会导致______.
(4)Na2S2O5与稀硫酸反应放出SO2,其离子方程式为______.
解:该原理为:反应Ⅰ为生成NaHCO3,加热生成Na2CO3,在反应Ⅱ中二氧化硫与碳酸钠反应生成NaHSO3与二氧化碳,加热NaHSO3生成Na2S2O5.
(1)工艺流程可知,反应Ⅰ为生成NaHCO3,氯化钠溶液通入氨气、二氧化碳生成碳酸氢钠与氯化铵,反应方程式为:CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl;
反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出,
故答案为:CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl;NH3;
(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;
由转化关系可知,反应中需要CO2、H2O,其它反应又生成的CO2、H2O,故CO2、H2O可以重复利用;
故答案为:增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;CO2、H2O;
(3)反应Ⅱ中发生反应Na2CO3+H2O+2SO2=2NaHSO3+CO2↑,2NaHSO3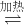 Na2S2O5+H2O,故SO2与Na2CO3的物质的量之比接近
Na2S2O5+H2O,故SO2与Na2CO3的物质的量之比接近
2:1恰好完全反应,若SO2不足Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低;
故答案为:2:1;Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水,反应离子方程式为:S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O.
分析:该原理为:反应Ⅰ为生成NaHCO3,加热生成Na2CO3,在反应Ⅱ中二氧化硫与碳酸钠反应生成NaHSO3与二氧化碳,加热NaHSO3生成Na2S2O5.
(1)工艺流程可知,反应Ⅰ为生成NaHCO3,氯化钠溶液通入氨气、二氧化碳生成碳酸氢钠与氯化铵,反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出;
(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;
反应需要的物质,在其它的反应中又生成该物质,该物质可以循环利用,结合方式的反应判断;
(3)反应Ⅱ中发生反应Na2CO3+H2O+SO2=2NaHSO3+CO2↑,2NaHSO3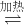 Na2S2O5+H2O,根据碳酸钠与二氧化硫能完全反应判断,二者物质的量关系;
Na2S2O5+H2O,根据碳酸钠与二氧化硫能完全反应判断,二者物质的量关系;
若SO2不足Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水.
点评:本题以制备焦亚硫酸钠为载体,考查学生对于工艺流程原理的理解、对操作与反应条件可知的理解,侯德榜制碱法、S与C等元素化合物的性质与转化、常用化学用语书写等,知识比较陌生,难度较大,理解制备原理是关键,需要学生具备扎实的基础与综合运用能力.
(1)工艺流程可知,反应Ⅰ为生成NaHCO3,氯化钠溶液通入氨气、二氧化碳生成碳酸氢钠与氯化铵,反应方程式为:CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl;
反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出,
故答案为:CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl;NH3;
(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;
由转化关系可知,反应中需要CO2、H2O,其它反应又生成的CO2、H2O,故CO2、H2O可以重复利用;
故答案为:增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;CO2、H2O;
(3)反应Ⅱ中发生反应Na2CO3+H2O+2SO2=2NaHSO3+CO2↑,2NaHSO3
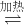 Na2S2O5+H2O,故SO2与Na2CO3的物质的量之比接近
Na2S2O5+H2O,故SO2与Na2CO3的物质的量之比接近2:1恰好完全反应,若SO2不足Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低;
故答案为:2:1;Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水,反应离子方程式为:S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O.
分析:该原理为:反应Ⅰ为生成NaHCO3,加热生成Na2CO3,在反应Ⅱ中二氧化硫与碳酸钠反应生成NaHSO3与二氧化碳,加热NaHSO3生成Na2S2O5.
(1)工艺流程可知,反应Ⅰ为生成NaHCO3,氯化钠溶液通入氨气、二氧化碳生成碳酸氢钠与氯化铵,反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出;
(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;
反应需要的物质,在其它的反应中又生成该物质,该物质可以循环利用,结合方式的反应判断;
(3)反应Ⅱ中发生反应Na2CO3+H2O+SO2=2NaHSO3+CO2↑,2NaHSO3
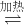 Na2S2O5+H2O,根据碳酸钠与二氧化硫能完全反应判断,二者物质的量关系;
Na2S2O5+H2O,根据碳酸钠与二氧化硫能完全反应判断,二者物质的量关系;若SO2不足Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水.
点评:本题以制备焦亚硫酸钠为载体,考查学生对于工艺流程原理的理解、对操作与反应条件可知的理解,侯德榜制碱法、S与C等元素化合物的性质与转化、常用化学用语书写等,知识比较陌生,难度较大,理解制备原理是关键,需要学生具备扎实的基础与综合运用能力.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素⑦中质子数和中子数相等的同位素符号是______.
(3)④、⑤、⑦的原子半径由大到小的顺序为______.
(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为______>______.
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为______.
(6)周期表中,同一主族元素化学性质相似;同时有些元素和它在周期表中左上方或右下方的另一主族元素的化学性质也相似,如Li与Mg,这称为对角线规则.上表中与铍的化学性质相似的元素有(填元素名称)______.铍的最高价氧化物对应水化物属于两性化合物,该化合物的化学式是______,能够说明其具有两性的反应离子方程式为:______;______.
Ⅱ.由表中①~⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答

(1)若X是强氧化性单质,则A不可能是______(填序号).
a.S b.N2 c.Na d.Mg e.Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属阳离子的化学试剂______,现象是______;又知在酸性溶液中该金属阳离子能被双氧水氧化,写出该反应的离子方程式:______.
(3)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为______,写出A与C两溶液反应的离子方程式:______.
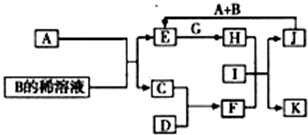 A-L为中学化学常见物质,其主要转化关系如图所示(其中产物水已略去).已知A为金属单质,C、D通常状况下为气体单质.B、F均为重要的化工产品,F为具有刺激性气味的气体,将一定量F通入B的稀溶液中可以得到两种盐K和L.G和I分别由相同的两种元素组成,通常状况下均为无色液体.
A-L为中学化学常见物质,其主要转化关系如图所示(其中产物水已略去).已知A为金属单质,C、D通常状况下为气体单质.B、F均为重要的化工产品,F为具有刺激性气味的气体,将一定量F通入B的稀溶液中可以得到两种盐K和L.G和I分别由相同的两种元素组成,通常状况下均为无色液体.