题目内容
如图表是元素周期表的一部分,请按要求回答以下问题:
(1)①和②形成的常见化合物有 (填化学式,填一种即可);
(2)在③~⑥中,原子半径最大的原子结构示意图是 ;
(3)④的单质与Fe2O3在高温下反应的化学方程式: ;
(4)②和⑤的单质中,氧化性较弱的是 (填化学式);
(5)⑤的一种氧化物可以与⑥的单质的水溶液发生氧化还原反应,生成两种强酸,写出该反应的化学方程式: .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(2)在③~⑥中,原子半径最大的原子结构示意图是
(3)④的单质与Fe2O3在高温下反应的化学方程式:
(4)②和⑤的单质中,氧化性较弱的是
(5)⑤的一种氧化物可以与⑥的单质的水溶液发生氧化还原反应,生成两种强酸,写出该反应的化学方程式:
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知①为C、②为O、③为Na、④为Al、⑤为S、⑥为Cl.
(1)①和②形成的常见化合物有一氧化碳、二氧化碳;
(2)在③~⑥中,原子半径最大的为Na,原子核外有11个电子,有3个电子层,各层电子数为2、8、1;
(3)Al与Fe2O3在高温下发生铝热反应,生成Fe与氧化铝;
(4)同主族自上而下元素非金属性减弱,单质氧化性减弱;
(5)⑤的一种氧化物可以与⑥的单质的水溶液发生氧化还原反应,生成两种强酸,为二氧化硫与氯水反应生成硫酸与盐酸.
(1)①和②形成的常见化合物有一氧化碳、二氧化碳;
(2)在③~⑥中,原子半径最大的为Na,原子核外有11个电子,有3个电子层,各层电子数为2、8、1;
(3)Al与Fe2O3在高温下发生铝热反应,生成Fe与氧化铝;
(4)同主族自上而下元素非金属性减弱,单质氧化性减弱;
(5)⑤的一种氧化物可以与⑥的单质的水溶液发生氧化还原反应,生成两种强酸,为二氧化硫与氯水反应生成硫酸与盐酸.
解答:
解:由元素在周期表中位置,可知①为C、②为O、③为Na、④为Al、⑤为S、⑥为Cl.
(1)①和②形成的常见化合物有一氧化碳、二氧化碳,对应化学式为CO、CO2,故答案为:CO或CO2;
(2)在③~⑥中,原子半径最大的为Na,原子核外有11个电子,有3个电子层,各层电子数为2、8、1,其原子结构示意图为: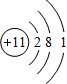 ,故答案为:
,故答案为: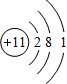 ;
;
(3)Al与Fe2O3在高温下发生铝热反应,生成Fe与氧化铝,化学反应方程式为:2Al+Fe2O3
2Fe+Al2O3,故答案为:2Al+Fe2O3
2Fe+Al2O3;
(4)同主族自上而下元素非金属性减弱,单质氧化性减弱,故氧化性O2>S,故答案为:S;
(5)⑤的一种氧化物可以与⑥的单质的水溶液发生氧化还原反应,生成两种强酸,为二氧化硫与氯水反应生成硫酸与盐酸,反应方程式为:SO2+Cl2+2H2O=H2SO4+2HCl,故答案为:SO2+Cl2+2H2O=H2SO4+2HCl.
(1)①和②形成的常见化合物有一氧化碳、二氧化碳,对应化学式为CO、CO2,故答案为:CO或CO2;
(2)在③~⑥中,原子半径最大的为Na,原子核外有11个电子,有3个电子层,各层电子数为2、8、1,其原子结构示意图为:
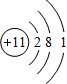 ,故答案为:
,故答案为: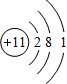 ;
;(3)Al与Fe2O3在高温下发生铝热反应,生成Fe与氧化铝,化学反应方程式为:2Al+Fe2O3
| ||
| ||
(4)同主族自上而下元素非金属性减弱,单质氧化性减弱,故氧化性O2>S,故答案为:S;
(5)⑤的一种氧化物可以与⑥的单质的水溶液发生氧化还原反应,生成两种强酸,为二氧化硫与氯水反应生成硫酸与盐酸,反应方程式为:SO2+Cl2+2H2O=H2SO4+2HCl,故答案为:SO2+Cl2+2H2O=H2SO4+2HCl.
点评:本题考查元素周期表与元素周期律应用,比较基础,注意元素周期表的掌握,侧重基础知识的巩固.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、铝与烧碱溶液反应:Al+2OH-═AlO2-+H2↑ |
| B、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
| C、少量CO2气体通入氢氧化钙溶液中:CO2+2OH -═CO32-+H2O |
| D、氯化铁溶液呈酸性:Fe3++3H2O?Fe(OH)3+3 H+ |
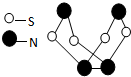 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图所示是已合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图所示是已合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A、该物质的分子式为SN |
| B、该物质与化合物S2N2互为同素异形体 |
| C、该物质在固态时形成原子晶体 |
| D、该物质的分子中既有极性键,又有非极性键 |
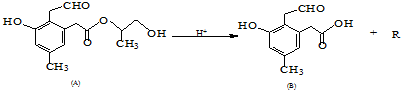
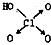
 (1)判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性就越强.含氧酸酸性强弱与非羟基氧原子数的关系如下表所示:
(1)判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性就越强.含氧酸酸性强弱与非羟基氧原子数的关系如下表所示: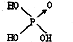
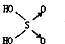


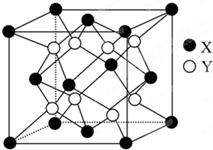 某离子晶体的晶体结构如图所示,试求:
某离子晶体的晶体结构如图所示,试求: