题目内容
下列关于化学键的说法中正确的是( )
| A、气体单质中一定含有共价键 |
| B、由非金属元素组成的化合物一定是共价化合物 |
| C、含有离子键的晶体一定是离子晶体 |
| D、一定是在发生化学反应时,化学键才发生断裂 |
考点:化学键
专题:化学键与晶体结构
分析:A.单原子分子中不含化学键;
B.由非金属元素组成的化合物可能是离子化合物;
C.含有离子键的晶体一定是离子晶体,离子晶体中可能含有共价键;
D.不一定发生化学变化时化学键才发生断裂.
B.由非金属元素组成的化合物可能是离子化合物;
C.含有离子键的晶体一定是离子晶体,离子晶体中可能含有共价键;
D.不一定发生化学变化时化学键才发生断裂.
解答:
解:A.单原子分子中不含化学键,如稀有气体中不含化学键,故A错误;
B.由非金属元素组成的化合物可能是离子化合物,如铵盐,故B错误;
C.含有离子键的晶体一定是离子晶体,离子晶体中可能含有共价键,如KOH,故C正确;
D.不一定发生化学变化时化学键才发生断裂,如电解质在水溶液中的电离,故D错误;
故选C.
B.由非金属元素组成的化合物可能是离子化合物,如铵盐,故B错误;
C.含有离子键的晶体一定是离子晶体,离子晶体中可能含有共价键,如KOH,故C正确;
D.不一定发生化学变化时化学键才发生断裂,如电解质在水溶液中的电离,故D错误;
故选C.
点评:本题考查化学键,侧重考查基本概念、基本理论,注意规律中的异常现象,易错选项是AD,注意:化学反应中一定发生化学键的断裂和形成,但发生化学键断裂不一定发生化学键形成,为易错点.

练习册系列答案
相关题目
下列分离和提纯的实验中,所选用的方法或仪器不正确的是( )
| 序号 | A | B | C | D |
| 实验目的 | 分离食盐水与泥沙 | 分离水和CCl4 | 制取蒸馏水 | 从浓食盐水中得到氯化钠晶体 |
| 分离方法 | 过滤 | 萃取 | 蒸馏 | 蒸发 |
| 选用仪器 | 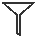 |  |  |  |
| A、A | B、B | C、C | D、D |
有下列试剂 ①KSCN ②淀粉-碘化钾溶液 ③Fe ④Cu ⑤H2S ⑥NH3?H2O ⑦Na2CO3溶液,和三氯化铁溶液反应时,使Fe 3+表现出氧化性的试剂有( )
| A、①⑥⑦ | B、②③④⑤ |
| C、④⑤⑥⑦ | D、全部 |
某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子,其物质的量浓度比为c(Na+):c(Mg2+):c(Cl-)=3:4:5,若Na+的物质的量浓度为3mol?L-1,则SO42-的物质的量浓度为( )
| A、2 mol?L-1 |
| B、3 mol?L-1 |
| C、4 mol?L-1 |
| D、8 mol?L-1 |
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法 |
已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11.下列说法正确的是( )
| A、25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B、25℃时,Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C、25℃时,Mg(OH)2固体在20 mL 0.01 mol?L-1氨水中的Ksp比在20 mL 0.01 mol?L-1NH4Cl溶液中的Ksp小 |
| D、25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
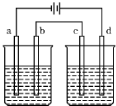 按图电解实验装置(都是惰性电极),若通直流电一段时间后,左池中溶液的pH上升,右池中溶液的pH下降,不仅a,b两电极放电离子的物质的量相等,且b,c两电极放电离子的物质的量也相等,则电解液应选用下表中的( )
按图电解实验装置(都是惰性电极),若通直流电一段时间后,左池中溶液的pH上升,右池中溶液的pH下降,不仅a,b两电极放电离子的物质的量相等,且b,c两电极放电离子的物质的量也相等,则电解液应选用下表中的( )