题目内容
7.(1)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液显碱性,发生反应的离子方程式为ClO-+2I-+H2O═I2+Cl-+2OH-.②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,写出发生反应的离子方程式SO32-+I2+2OH-═SO42-+2I-+H2O.
③对比①和②实验所得的结果,将I2、ClO-、SO42-按氧化性由强到弱的顺序排列为ClO->I2>SO42-.
(2)今有铁皮、铜片、酸、碱、盐溶液若干.设计实验证明以下事实,写出反应的化学方程式.
①浓硫酸的氧化性比稀硫酸强:Cu与浓H2SO4在加热时反应而与稀H2SO4在加热时不反应;Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强:Cu与FeCl3溶液能反应;2FeCl3+Cu═2FeCl2+CuCl2.
③铁的还原性比铜强:Fe能与CuSO4溶液反应置换出Cu;Fe+CuSO4═FeSO4+Cu.
分析 (1)次氯酸钠具有强氧化性,可氧化I-生成单质I2,I2遇淀粉变蓝;Na2SO3具有还原性,可还原I2生成I-,使蓝色消失,离子方程式的书写思路是:确定反应物、产物,然后根据电子得失守恒和电荷守恒配平,氧化还原反应中,氧化剂氧化性大于氧化产物的氧化性;
(2)①可根据Cu和浓H2SO4加热反应,而Cu和稀H2SO4加热也不反应来证明;②③可利用氧化还原方程式来证明.
解答 解:(1)①次氯酸钠具有强氧化性,可氧化I-生成单质I2,I2遇淀粉变蓝,反应的离子方程式为ClO-+2I-+H2O═I2+Cl-+2OH-,
故答案为:ClO-+2I-+H2O═I2+Cl-+2OH-;
②Na2SO3具有还原性,可还原I2生成I-,使蓝色消失,反应的离子方程式为SO32-+I2+2OH-═SO42-+2I-+H2O,
故答案为:SO32-+I2+2OH-═SO42-+2I-+H2O;
③氧化还原反应中,氧化剂氧化性大于氧化产物的氧化性,由①可知ClO->I2,由②可知I2>SO42-,
故答案为:ClO->I2>SO42-.
(2)①Cu和浓H2SO4加热反应,而Cu和稀H2SO4加热也不反应,则可说明浓硫酸氧化性大于稀硫酸,反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu与浓H2SO4在加热时反应而与稀H2SO4在加热时不反应;Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
②Cu与FeCl3溶液能反应:2FeCl3+Cu═2FeCl2+CuCl2,氧化剂氧化性大于氧化产物的氧化性,则可证明氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强,
故答案为:Cu与FeCl3溶液能反应;2FeCl3+Cu═2FeCl2+CuCl2;
③Fe能与CuSO4溶液反应置换出Cu,符合活泼金属置换出不活泼金属的原则,Fe+CuSO4═FeSO4+Cu,可证明铁的还原性比铜强,
故答案为:Fe能与CuSO4溶液反应置换出Cu;Fe+CuSO4═FeSO4+Cu.
点评 本题综合考查了氧化还原反应、元素化合物的性质等,侧重于考查学生的实验设计能力,注意把握相关物质的性质,题目难度不大.

 名校课堂系列答案
名校课堂系列答案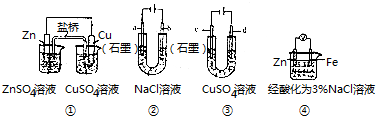
| A. | 装置①中,盐桥(含有琼胶的KCl饱和溶液)中的K+移向ZnSO4溶液 | |
| B. | 装置②工作一段时间后,a极附近溶液的pH减小 | |
| C. | 用装置③精炼铜时,c极为纯铜 | |
| D. | 装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
| A. | 铝 | B. | 铁 | C. | 镁 | D. | 锌 |
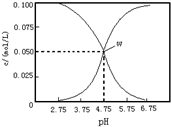
| A. | 该温度下醋酸的电离平衡常数为ka=10-4.75 | |
| B. | pH=6的溶液中,c(K+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L | |
| C. | pH=3.75的溶液中c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | 向W点所示溶液中通入0.1molHCl气体(溶液体积可以忽略不计)c(H+)=c(OH-)+c(CH3COOH) |
| A. | 用乙醚从黄花蒿中提取青蒿素 | B. | 用氯化铁溶液腐蚀铜制印刷电路板 | ||
| C. | 空气净化器中用活性炭层净化空气 | D. | 用热的纯碱溶液去除油污 |
| A. | 向漂白液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- | |
| B. | 用氨水吸收足量二氧化硫:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 用足量的氧氧化钠溶液吸收二氧化氮:3NO2+2OH-═2NO3-+NO+H2O | |
| D. | 次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
( )
| A. | 13 | B. | 14 | C. | 15 | D. | 不能确定 |
| A. | 标准状况下,11.2LCHCl3含有共价键数为2NA | |
| B. | 某温度下,纯水pH=6,该温度下1LpH=11的NaOH溶液中含有OH-数目为0.1NA | |
| C. | 含3.65gHCl的水溶液中含有粒子数为0.2NA | |
| D. | 0.2mol/LNa2S溶液中含有S2-数目小于0.2NA |
| A. | H2S的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | S2-的结构示意图: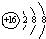 | |
| C. | Na2O2的电子式:Na+[$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$]2-Na+ | |
| D. | CCl4的电子式: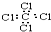 |